Sinonasal patologi · 2019-03-14 · Sinonasal patologi Svetlana Tafjord – OUS, 8. februar 2018...
Transcript of Sinonasal patologi · 2019-03-14 · Sinonasal patologi Svetlana Tafjord – OUS, 8. februar 2018...
Sinonasal patologi
Svetlana Tafjord
OUS, 8. februar 2018
Sinonasal patologi
• Lite anatomisk område
• Stor variasjon av non neoplastiske og neoplastiske lesjoner:
– Oppstår utelukkende/oftest i sinonasal region
– Oppstår andre steder, også i sinonasal region
Atlas of Head and Neck Pathology 2016, Bruce M. Wenig
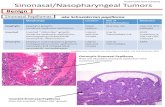
Histologi: Pseudoflerradet ciliert epitel med spredte mukøse-/begerceller Godt vaskularisert stroma Lobulær anordning av seromukøse kjertler
Atlas of Head and Neck Pathology 2016, Bruce M. Wenig
Sinonasale polypper Årsak
• Infeksjon, allergi, diabetes, Aspirin intoleranse, cystisk fibrose
• Voksne >20 år, sjeldent barn < 5år
Symptomer
• Nesetetthet, sekret fra nese hodepine
Histologi
• Polypøs form
• Regelmessig pseudoflerradet sylindrisk epitel evt. metaplastisk plateepitel
• Tap av seromukøse kjertler i stroma
• Inflammatorisk infiltrat (lymfocytter, plasmaceller med eller uten eosinofile)
• Stroma kan vise myxoid degenerasjon, sirkulasjonsforstyrrelse, fibrinutfelling
• Spredte fyldige fibroblaster
Rikshospitalet arkiv
Sinonasale polypper med soppinfeksjon
• Ofte eksudat med rikelig mengde inflammatoriske celler, deriblant eosinofile
• For øvrig lignende histologisk bilde som ved nesepolypper
• Oftest Aspergillus, av og til som små misfargete knuter «aspergilom»
• Immunsuprimerte kan ha infeksjon med Mucor sp.
• Antistoff mot Aspergillus og Mucor
Biopsi fra neseslimhinne ved rheumatologisk/autoimmun sykdom
• Pasienter med kronisk sykdomsbilde
• Uspesifikke symptomer fra øvre luftveier
• Positiv serologi (ANCA, ACE, SR)
• Lite funn i neseslimhinnen, evt. ulcerasjon
• Tegn til nyreaffeksjon (høy kreatinin, hyperkalcemi)
• Ofte spørsmål om sarkoidose, granulomatøs polyangiit, Churg- Strauss sykdom
Granulomatøs betennelse • Krever god representativ biopsi av en viss tykkelse (obs!
vurdering av vaskulitt i kar et stykke unna ulcerasjon)
• Funn av epiteloide granulomer er uspesifikt – Infeksjon (sopp, syrefaste staver, obs! spesialfarginger og
mikrobiologisk undersøkelse) – Sarkoidose – Granulomatøs polyangiit, Churg – Strauss (eosinofili) – Fremmedlegemer/medisiner, stoffer
• Neseslimhinne, ofte uten bevart overflateepitel • Redusert mengde normale spyttkjertler • Kronisk betennelse med eller uten eosinofili • Epiteloide granulomer med eller uten nekrose • Vaskulitt
Granulomatøs betennelse Histologi
• Tap av små spyttkjertler
• Kronisk betennelse
• Relativt veldefinerte granulomer – Runde eller avlange
– Histiocytter, makrofager, betennelsesceller
• Uten nekrose
Dg. Respiratorisk slimhinne med kronisk granulomatøs betennelse uten nekrose.
Rikshospitalet arkiv
Granulomatøs betennelse
Histologi
• Tap av små spyttkjertler
• Stroma med avlange granulomer med perifer palisadering av histiocytter
• Flerkjernete kjempeceller
• Sentralt henfall/nekrose
• Kar med eller uten vaskulitt – Fibrinoid veggnekrose
– Ekstravasering av erytrocytter
– Betennelsesceller i veggen Rikshospitalet arkiv
Vaskulitt Histologi
• Tydelige forandringer
• Transmural betennelse
• Fibrinoid veggnekrose
• Ekstravasering av erytrocytter
• Med eller uten eosinofili (Churg-Strauss)
• Ofte ulcerasjon
Atlas of Head and Neck Pathology 2016, Bruce M. Wenig
Proliferative epiteliale lesjoner i sinonasalt tractus
Non neoplastiske
• Respiratorisk epitelialt adenomatoid hamartom (REAH)
• Seromukøst hamartom
(SMH)
Neoplastiske
• Invertert «Schneideriansk» papillom
• Lavgradig sinonasalt adenokarsinom
Inflammasjon ? Neoplasi?
Respiratorisk Epitelial Adenomatoid Hamartom (REAH) • Usikker etiologi: inflammatorisk?
• Ofte assosiert med kronisk rhinosinusitt og nesepolypper
• Neoplastisk etiologi diskuteres • Voksne, oftere menn
Symptomer: • Nasal obstruksjon, sekret, hodepine Histologi: • Polypøs lesjon • Regelmessig pseudoflerradet
sylindrisk overflateepitel • Tap av ordinære seromukøse kjertler • Proliferasjon av dilaterte kjertler
kledd av samme type epitel som på overflaten
• Hyalinisert basalmembran • Kronisk betennelse • Kan være assosiert med ordinære
nasale polypper
Rikshospitalet arkiv
Seromucinøst hamartom • Usikker etiologi • Lik kjønnsfordeling • Polypøs masse
Symptomer: • Nasal obstruksjon, blødning,
evt. tilfeldig funn
Histologi: • Proliferasjon av små kjertler
kledd av en epitel rad – CK7+, CK19+, S-100+, tap av
basalcellelag
• Små kjertler kan «utgå» fra større «cilierte» kjertler
• Tilfeldig distribuerte kjertler eller lobulær anordning
• Lite stroma mellom kjertlene • Stroma myxoid, fibrøst
Atlas of Head and Neck Pathology 2016, Bruce M. Wenig
Klassifisering av neoplasmer i sinonasalt tractus
Atlas of Head and Neck Pathology 2016, Bruce M. Wenig
Schneideriansk papillom • Neoplastisk, benign epitelial
proliferasjon av slimhinne i sinonasalt tractus
• Eksponering for løsemidler over tid • Ca. 40 % HPV relatertHPV6/11 og HPV16/18
Symptomer • Uspesifikke: neseblødning, nasal
obstruksjon, sekret, hodepine
Morfologi • Polypøs masse, ofte hardere enn
inflammatoriske nesepolypper, bølgete overflate (morbærtre lignende)
• Lokal destruerende vekst
Histologi • Invertert, exofytisk, onkocytær variant • Polypøs lesjon • Flerradet epitel på overflaten med
invertert vekst i stroma (plateepitel, metaplastisk epitel, evt. onkocytært)
• Spredte begerceller • Kronisk aktiv betennelse i stroma og
intraepitelialt • Typiske mikroabscesser intraepitelialt • Ingen dysplasi
Rikshospitalet arkiv
Rikshospitalet arkiv
Schneideriansk papillom med dysplasi • Opptil 20 % kan gjennomgå
malign transformasjon • <3% ikke røykere/25% røykere • HPV6/11 versus HPV16 • Dysplasi - ca. in situ -
infiltrerende plateepitelkarsinom
• Utbredt vekst • Dysplasi kan være vanskelig å
vurdere, ofte skrått skåret epitel
Histologi • Tydelig økt celletetthet • Hyperkromatiske, tettliggende
kjerner • Økt N/C ratio • Tap av begerceller • Tap av mikroabscesser i
epitelet
Rikshospitalet arkiv
Karsinom ex. Schneideriansk papillom • Plateepitelkarsinom
– Mucoepidermoid
– Spolcellet PEC
– Småcellet ca.
– Sinonasalt udifferensiert ca.
• Ofte koeksisterende invertert papillom og dysplasi
• Tap av polypøs arkitektur
• Tett stroma/desmoplastisk
• Tydelig infiltrerende vekst
• Kirurgi og strålebehandling
Rikshospitalet arkiv
Sinonasalt meningeom • Benign tumor utgående fra
meningoteliale celler • Primær ektopisk meningeom
– Ingen kontakt med CNS
• Sekundær ektopisk meningeom – Kontakt med CNS
• Oftest nese og paranasale bihuler, sjeldent frontal sinus eller nasopharynx
• Uspesifikke symptomer • Kan vokse lokaldestruktivt og
etterligne malign tumor Histologi • Lobulært vekst med tumorreder
adskilt av bindevev • Celler med utydelige grenser,
blekt cytoplasma runde til ovale kjerner og virvlet utseende
• Kjerner med inklusjoner Immunhistokjemi
– EMA+, PGR+, D2-40+
EMA PGR D2-40
Rikshospitalet arkiv
MALIGNE SVULSTER I SINONASAL TRACTUS
Atlas of Head and Neck Pathology 2016, Bruce M. Wenig
Sinonasalt adenokarsinom
• 10-20 % av alle primære sinonasale maligne svulster
• 6,3 % uten spyttkjertelkarsinomer
• Intestinal variant • Non intestinal variant
– Lavgradig malign – Høygradig malign
• (Metastase)
Intestinalt sinonasalt adenokarsinom
• 500 ganger høyere prevalens hos personer som over tid har vært eksponert for løsemidler eller jobbet i treindustri
• Symptomer – Nasalobstruksjon, epistaxis, sekresjon
• Histologi – Samme spektrum som intestinalt
adenokarsinom (colon type, solid, mucinøs, blandet)
– Proliferasjon av kjertler, tubuli, villi kledt av sylindrisk, kubisk, signet ring eller, mucinøst epitel
• Immunhistokjemi • CK20+, CDX2+, CK7-(+)
• Cytogenetiske og molekylære funn – K- ras 25%, h ras sporadisk – Mikrosatelitt instabilitet: ikke til
stede – CGH varierte «gains» og «losses»
Malign epitelial glandulær neoplasme, morfologisk og immunhistokjemisk lik intestinalt adenokarsinom
Rikshospitalet arkiv
CDX2 CK20 CK7
CDX2 CK7
Lavgradig malignt sinonasalt adenokarsinom (non intestinalt)
• Svært sjelden, stor aldersspenn
• Ukjent etiologi
• Symptomer: uspesifikke
• Polypøs fast masse
Histologi • Papillær, tubulær, komplekst vekst
• Rygg mot rygg kjertler
• Lite stroma
• Enradet epitel, kubisk til sylindrisk
• Lite cytologisk atypi
• Klarcellet komponent; obs metastase fra RCC
Immunhistokjemi – CK7+
– P63- (evt. fokal)
– CK20-, CDX2- (evt. svak fokal)
CK7 CK5/6, CK20, CDx2
Rikshospitalet arkiv
Lavgradig malign epitelial tumor med glandulær differensiering uten intestinal eller spyttkjertel differensiering
Høygradigmalignt sinonasalt adenokarsinom (non intestinalt)
• Høygradig malign epitelial tumor med glandulær differensiering uten intestinal eller spyttkjertel differensiering
• Noe hyppigere i sinus maxillaris • Ingen kjente etiologiske faktorer
Symptomer
– Neseobstruksjon, epistaxis, smerte, ansiktsasymmetri
Histologi
– Infiltrerende vekst, oftere solid, men også glandulært og papillært
– Cytologisk atypi, moderat til grov – Forhøyet mitotisk aktivitet/nekrose
Immunhistokjemi – Alltid CK7+ – Negativ for CK20, CDX2 – Negative endokrine markører – Som oftest negative myoepiteliale
markører (p63, SMA, CK5/6)
CK7
CK20
Ki67
Sinonasalt plateepitelkarsinom
Keratiniserende
• 80-85% av alle PEC i dette området
• Økt insidens hos røykere og ved høyt alkoholinntak
• Ikke HPV relatert
• Høyt, middels og lite differensiert, identisk med konvensjonelt PEC
Non keratiniserende
• En del HPV relatert
• Ikke assosiert med røyking eller høyt alkoholinntak
• Malign epitelial tumor utgått fra overflateepitel med plateepiteldifferensiering • Hyppigst malign tumor i sinonasal tractus
Sinonasalt plateepitelkarsinom keratiniserende
• B. atypiske men tydelige plateepitelceller – Moderat til rikelig mengde
cytoplasma – Forstørrete atypiske kjerner – Nukleoler – Keratinisering
• C. fortsatt tydelig plateepiteldifferensiering – Fortetning av kjerner – Mer atypi – Hyppigere mitoser – Mindre keratinisering
• D. begrenset eller lite plateepiteldifferensiering – Dyskeratotiske enkeltceller – Mørkere kjerner – Høy mitotisk aktivitet – Apoptose/nekrose
Foto B, C, D Atlas of Head and Neck Pathology 2016, Bruce M. Wenig
Sinonasalt plateepitelkarsinom non keratiniserende • C.
– in situ komponent fra non- keratiniserende PEC
• D. – Avlange, mørke celler – Basofile, tettliggende kjerner – Vokser som bånd og solide flak
• E.
– Lite differensiert tumor – Primitiv utseende – Ingen synlig
plateepiteldifferensiering – Krever relativt utbredt
immunhistokjemi • Plateepitelfenotype
– CK5/6+, p40+, p63+, CK7- (evt. svak, fokal +)
Foto C, D,E Atlas of Head and Neck Pathology 2016, Bruce M. Wenig
Udifferensierte maligne svulster i sinonasal tractus
differensialdiagnostisk tilnærming
Modern Pathology (2017) 30, S1–S26; doi:10.1038/modpathol.2016.119
Surgical Pathology 10 (2017) 103–123, http://dx.doi.org/10.1016/j.path.2016.10.005
• Ikke alltid «rundcellet» • Ikke alltid småcellet • Ikke alltid «blå» • Alltid udifferensierte
1 2 3
4 5 6
7 8 9
10 11 12
Foto 10,11,12: Atlas of Head and Neck Pathology 2016, Bruce M. Wenig
1 Diffust storcellet B celle lymfom
Kun kjemoterapi
2 Plasmocytom ekstraskeletalt Kun kjemoterapi
3* Malignt melanom (mucosalt) Kirurgi, evt. immunterapi
4* Sinonasalt udifferensiert karsinom SNUC Primær stråleterapi
5 Rhabdomyosarcom Primær kjemoterapi etter RMS protokoll
6* Olfaktorisk neuroblastom Primær kirurgi
7 Sinonasalt non keratiniserende plateepitelkarsinom
Primær kirurgi
8* SMARCB21 (INI1) «deficient» sinonasalt karsinom
Primær kirurgi
9* NK-T celle lymfom Kun kjemoterapi
10 EWING sarcom Primær kjemoterapi etter Ewing protokoll
11* NUT karsinom (midtlinje) Kjemoterapi, radioterapi
12 Småcellet neuroendokrint karsinom Kjemoterapi
Olfaktorisk (esthesio) neuroblastom
Malign neuroektodermal tumor utgående fra olfaktorisk membran i sinonasal tractus
Olfaktorisk neuroblastom
• Sjelden tumor (2-3% av alle sinonasale svulster)
• Pasienter i alle aldre, likt fordelt på begge kjønn
• Tumormasse i øvre del av nasalkavitet, ofte med affeksjon av bihuler
• Symptomer primært unilateral nasalobstruksjon, sjeldnere smerte og neurologisk utfall
Foto C: Atlas of Head and Neck Pathology 2016, Bruce M. Wenig
Histologi Immunhistokjemi
• Positive – Synaptofysin
– S-100 i støtteceller
• Negative – CK
Olfaktorisk neuroblastom
• Lobulær vekst: reder av tumorceller adskilt av fibrovaskulære septa
• Støtteceller rundt reder
• Tumorceller med runde, jevnstore kjerner med små nukleoler
• Neurofibrillær matrix, neuropil
• Økende kjernepleomorfi, mindre neuropil, flere mitoser og nekroser fra grad 1 til grad 4 etter Hyem
CK
Synaptofysin
S-100
Rikshospitalet arkiv
Foto; Atlas of Head and Neck Pathology 2016, Bruce M. Wenig
Grad I Grad II
Grad III Grad IV
Sinonasalt udifferensiert karsinom SNUC
• Hyppigere hos menn
• Stort aldersspenn
• Utbredt sykdom ved dg. – Nese, bihule orbita,
skallebasis, hjerne
– Symptomer avhengig av utbredelse
• Klinisk kort varighet
• Ukjent etiologi
• Histologi
• Variasjon i vekstmønster – Solid, trabekulær, lobulær
• Celler med liten mengde cytoplasma (høy n/c ratio)
• Kjerner mørke eller vesikuløse
Mitoser, apoptose, nekrose
Høygradig malignt udifferensiert karsinom uten kjertel- eller plateepiteldifferensiering
Atlas of Head and Neck Pathology 2016, Bruce M. Wenig
SNUC immunhistokjemi
• Positive
– AE1/AE3, CK, (CK7, CK8, CK19), INI1
• Negative
– CK5/6, CD45, NUT, EBV melanocyttmarkører, muskelmarkører
• Fokal/svak
– Synaptofysin, chromogranin, CD56, p63, p40
Behandling/prognose
• Multimodal behandling: radioterapi, kjemoterapi evt. kirurgi, avhengig av stadium
• 5 års overlevelse 32-43 %
• Residiv vanlig
CK
Rikshospitalet arkiv
Mucosalt malignt melanom • 0.5-3% av alle MM i alle
lokalisasjoner
• Tumor i voksen alder
• Symptomer – Luftveisobstruksjon
– Neseblødning
– Smerte
– Ulcerasjon som ikke gror
• Tumormasse kan være – Polypøs
– Bredbaset
– Ulcerert
• Histologi – Solide, løse flak, evt.
dissosierte celler
– Polygonale, epiteloide til plasmacytoide celler, spolcellet variant
– Pigment ikke alltid tilstede
Rikshospitalet arkiv
Malign tumor utgående fra melanocytter
Mucosalt malignt melanom immunhistokjemi
• Positive – Melan A, HMB45, S-100 ,
SOX10, MITF
– Spolcellet, desmoplastisk variant kan uttrykke kun S-100 og SOX 10 (obs! dd. andre spolcellete maligne svulster)
• Negative – CK, EMA; endokrine markører,
muskelmarkører, CD45
Molekylært funn – <20% har BRAF mutasjon og
c-kit mutasjon
– Hyppigere NRAS mutasjon
Behandling • Kirurgisk • Immunoterapi dersom påvist
genmutasjon
CK CD45 Melan A Melan A
Rikshospitalet arkiv
NUT midtlinjekarsinom • Hyppigere hos menn • Yngre pasienter (3-35 år) • Hyppigst i sinonasal tractus,
men også andre lokalisasjoner i hode hals
• Midtlinje – Thorax (mediastinum, thymus,
lunge, trachea) – Urinblære
• Ikke assosiert med HPV eller EBV
• Histologi – Lite differensiert karsinom med
spredt keratinisering – Celler med runde til ovale
irregulære kjerner, tydelige nukleoler
– Cytologisk atypi varierer – Liten mengde cytoplasma – Mitotisk aktiv
Karsinom med plateepitel- differensiering samt translokasjon av NUT genet («NUT» nukleær protein i testis)
Atlas of Head and Neck Pathology 2016, Bruce M. Wenig
NUT midtlinje karsinom
Immunhistokjemi:
• Positive – NUT (kjernepositiv), CK, INI1
EMA, CK5/6, p63, CK7, CK20
• Kan være positive – P40, CD34, Synaptofysin
• Negative – CD45, melanocytt- og
muskelmarkører, chromogranin, CD56
• Behandling – Multikjemoterapi, radioterapi
• Prognose – Dårlig, overlevelse <1år
NUT
Atlas of Head and Neck Pathology 2016, Bruce M. Wenig
SMARCB1 (INI1) «deficient»
sinonasalt karsinom • SMARCB1 «deficient»
tumorfamilie – Malign rabdoid tumor/ART
– Epiteloid sarkom
– Medulært nyrekarsinom
– Myoepitelialt karsinom i bløtvev
– Epitelioid MPNST
• Voksne, oftere kvinner
• Histologi – Udifferensiert tumor uten
plate- eller glandulær differensiering
– Basofil utseende
– Liten mengde cytoplasma
– Mitotisk aktiv, nekrose vanlig
Udifferensiert karsinom karakterisert av tap av SMARCB1 (INI1) uttrykk Forårsaket av delesjoner eller mutasjoner av SMARCB1 lokus
Rikshospitalet arkiv
SMARCB1 (INI1) «deficient»
sinonasalt karsinom; immunhistokjemi
• Positive – CK, CK5/6, p63, CK7,
synaptofysin (+/-)
• Negative – INI1 (tap av kjernefarging)
– NUT, chromogranin
• Behandling – Kirurgi, strålebehandling
• Prognose – Avhenger av stadium
– Residiv vanlig
– Metastaser til regionale lymfeknuter og distale metastaser/lunge, lever
p63 CK7 INI1
Rikshospitalet arkiv
Hvor begynne?
• Til tross for udifferensiert morfologi, se nøye etter
– Vekstmønster
• Solid, dissosiert
– Kjernemorfologi
• Uniforme, kantete, mørke
– Dyskeratotiske celler
– Pigment
– Neuropil
– Rabdomyoblast diff.
– Plasmacytoid diff.
Basert på morfologi begynn med
– CK, CD45, Melan A, Myogenin,
Synaptofysin, S-100, (CD99, CD138)
– Lurt å fordele biopsimateriale på flere blokker
CK positive – Karsinom
CK som regel negative – Malignt melanom, lymfom,
– Ewing, Rhabdomyosarcom, Olfaktorisk neuroblastom • CK positivitet kan forekomme !
Karsinomer (CK+)
Negative markører:
• Melan A,(HMb45/S-100),
• CD45
• Myogenin
• CD138
SMARCB1 «deficient» karsinom
CK+, INI1-, (CK5/6+-, p63+ ) NUT+
Sinonasalt udiff. karsinom (SNUC)
CK+, CK7+, Synapto+, INI1+
CK5/6-, p63-/+, NUT-
NUT karsinom
CK+, CK5/6+, p40+, NUT+
INI1+
Småcellet neuroend. ca CK+, Synapto fysin ++, Chromogranin++ , Ki67+++ CK7+-, CK20+-, TTF1+-CK5/6-+ INI1+, NUT-
Plateepitelkarsinom CK5/6+, p40+, INI1+ CK7-, NUT-, Synapto -