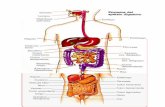
aparato repirato
-
Upload
rosario-villanueva -
Category
Documents
-
view
241 -
download
0
Transcript of aparato repirato

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 1/54
N E U M O L O G I A
P E D I A T R I C A
SOCIEDAD CHILENA DE NEUMOLOGIA PEDIATRICA
2008 Volumen 3 Número 2 Páginas 148-19SSN 0718-3321 (versión impresa)
Disponible en http://www.neumologia-pediatrica.cl
SSN 0718-333X (versión en línea)
CONTENIDO
• Desarro llo pulmonar
• Determinación de volúmenes
pulmonares
• Neumonía asociada a ventilación
• Tuberculos is y S IDA
• Mini s imposio VRS
Organo Oficial de la Sociedad Latinoamericana de Neumología Pediátrica

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 2/54
Revista NEUMOLOGIA PEDIATRICA
La Revista NEUMOLOGIA PEDIATRICA de la Sociedad Chilena de Neumología Pediatría, órgano oficial de laSociedad Latinoamericana de Neumología Pediátrica, publica artículos relevantes con la Salud Respiratoria Infantily del Adolescente; dirigida principalmente a médicos generales, familiares, pediatras, subespecialistas en medicinarespiratoria, kinesiólogos y enfermeras, con especial interés en aspectos clínicos, diagnósticos y terapéuticos. ElComité Editorial revisa cuidadosamente los trabajos enviados a nuestra sección y selecciona aquellos que brindan
temas de revisión, controversia o actualidad científica. Nuestro propósito es difundir conceptos actuales y herramientas
clínicas para una práctica médica adecuada con nuestros pequeños pacientes.
Editor Responsable
Dr. Luis Enrique Vega-BriceñoPediatra Broncopulmonar Departamento de PediatríaPontificia Universidad CatólicaSantiago de Chile, Chile
Cuerpo Editorial
Dr. José A. Castro-RodriguezPediatra Broncopulmonar Profesor Auxiliar Pontificia Universidad CatólicaSantiago de Chile, Chile
Dra. Ilse ContrerasPediatra Broncopulmonar Hospital Padre HurtadoSantiago de Chile, Chile
Dr. Luis Miguel FranchiNeumólogo PediatraPediatras AsociadosLima, Perú
Dr. Oscar FielbaumPediatra Broncopulmonar Profesor Asistente de Pediatría Universidad de ChileCentro Resiratorio PediátricoClínica las CondesSantiago de Chile, Chile
Dr. Cristián GarcíaRadiólogo InfantilProfesor Titular de RadiologíaDepartamentos de Radiología y PediatríaPontificia Universidad CatólicaSantiago de Chile, Chile
Dr. Manuel GutiérrezNeumólogo PediatraProfesor Asociado de PediatríaUniversidad Peruana Cayetano HerediaLima, Perú
Dr. Fernando IñiguezPediatra Broncopulmonar Hospital Base Puerto MonttPuerto Montt, Chile
Dr. Viviana LezanaPediatra Broncopulmonar Profesor Auxiliar Universidad de ValparaísoHospital Auxiliar - Hospital Doctor Gustavo Fricke Valparaíso, Chile
Dr. Rodrigo ParraRadiólogo InfantilProfesor Auxiliar de RadiologíaDepartamento de RadiologíaPontificia Universidad CatólicaSantiago de Chile, Chile
Dr. Carlos RodríguezNeumólogo PediatraBogotá, Colombia
Dr. Iván StandNeumólogo PediatraClínica de los Andes ISSDocente Universidad del NorteBarranquilla, Colombia
Dr. Renato SteinNeumólogo PediatraDepartamento de PediatríaPontifícia Universidad Católica de Río GrandePorto Alegre, Brasil
Dr. Alejandro Teper Neumólogo PediatraHospital de Niños Ricardo GutiérrezBuenos Aires, Argentina
Dr. Santiago VidaurretaNeumólogo PediatraHospital de Niños Ricardo GutiérrezBuenos Aires, Argentina
Editor Gráfico
Fernando Suárez J.Laboratorio Boehringer Ingelheim

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 3/54

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 4/54

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 5/54
disponible en http://www.neumologia-pediatr ica.cl
EDITORIAL
Uno de los aspectos respiratorios que plantea desafíos es la comprensión del desarrollo pulmonar que experimentan los niños.
Muchos eventos que ocurren en la vida fetal e infancia tienen una influencia directa en diversas enfermedades respiratorias
crónicas, incluso en adultos. Como es sabido, el desarrollo pulmonar no termina con el nacimiento; por el contrario, este
continúa en la vida extrauterina y se prolonga incluso hasta la edad escolar. Durante la última década se han publicado numerosas
investigaciones en torno a ello que han intentado explicar el complejo proceso de la vasculogénesis y el rol de diversas
citoquinas involucradas. En este número de la revista, me permito presentarles una interesante revisión de este apasionante
tema.
La determinación de volúmenes pulmonares es una herramienta muy útil para medir y cuantificar la severidad de muchas
enfermedades pulmonares crónicas en niños. Lamentablemente, cuando deseamos establecer si el valor obtenido por nuestro
instrumento es “normal”, caemos necesariamente en la ociosa pregunta de ¿con quién estamos comparando? o ¿que ecuación
estamos empleando?. La literatura recomienda que -idealmente- cada centro o laboratorio tenga sus propias ecuaciones a
partir de sujetos con características similares. Les presentamos una interesante revisión que no puede dejar de leer.
La sobrevida de muchos pacientes pediátricos es uno de los grandes retos que enfrentan cada día las unidades de cuidados
intensivos. La neumonía asociada a ventilación mecánica es una de las complicaciones más temidas; no sólo prolonga la estadía
hospitalaria sino que incrementa la morbimortalidad. Por otra parte, muchos médicos creían -erróneamente- que la tuberculosis
(TBC) era un problema controlado. Durante las últimas dos décadas se ha observado una explosión a nivel mundial en el
número de pacientes con TBC y SIDA. Existe evidencia que demuestra que la infección por el virus de inmunodeficiencia
humano determina un incremento del riesgo de TBC hasta en 7 veces más que los controles. Les presentamos dos revisiones
en torno infecciones intrahospitalarias asociadas a ventilación mecánica y otra de tuberculosis y SIDA en niños.
A principios de mayo del presente año, tuvimos la oportunidad de asistir a las V Jornadas para Especialistas organizadas por
la Sociedad Chilena de Neumología Pediátrica. El tema elegido para este año por podía ser menos interesante para los
pediatras: Novedades en VRS. En este número, les presentamos un breve resumen de estas conferencias, en donde la calidad
de los invitados extranjeros fue envidiable.
Esperamos que el lector, disfrute de este nuevo número de la revista que con mucho entusiasmo hemos preparado para uds.
Afectuosamente,
Luis E. Vega-BriceñoEditor Responsable

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 6/54

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 7/54
Resumen
El desarrollo pulmonar es un proceso complejo y altamente organizado, en el que se reconocen varias etapas dinámicas: embrionaria, pseudoglandular, canalicular, sacular, alveolar, maduraciónmicrovascular, hiperplasia activa e hipertrofia. El desarrollo de la vía aérea es seguido de modoestrecho por el desarrollo de la vasculatura pulmonar, para concluir en la formación de la unidadalvéolo-capilar. Todos estos procesos se encuentran controlados estrechamente por factores genéticos, tales como factores de crecimiento y otras moléculas, de acción sólo parcialmente comprendida.Para alcanzar un normal desarrollo, son fundamentales los movimientos respiratorios fetales, unadecuado espacio intratorácico, fluido intra y extrapulmonar en volumen suficiente y una adecuadairrigación y nutrición. Durante los procesos de organogénesis pueden ocurrir diversas alteraciones,debidas a factores materno-fetales, genéticos o ambientales, originando así anomalías del desarrollo, tanto en el período prenatal como postnatal. La respiración fetal y el fluido pulmonar juegan un papelimportante en la delicada relación entre los epitelios de la vía aérea y el mesénquima, al promoverel crecimiento pulmonar. Los movimientos respiratorios son fundamentales en la preservación del volumen pulmonar. Se postula que las contracciones peristálticas espontáneas de la vía aérea, favorecen la expansión de los brotes pulmonares al fac ilitar su crecimiento hacia el mesénquimacircundante. Los corticoides, administrados en el período pre o postnatal, aceleran el crecimientopulmonar por variados mecanismos, a costa de acortar el período de formación de los septos ydisminuir el número final de alvéolos.
Palabras Claves: Desarrollo pulmonar, organogénesis, pulmón, vía aérea.
disponible en http://www.neumologia-pediatrica.cl 148
NEUMOLOGIA PEDIATRICA ISSN 0718-3321
Desarrollo pulmonar Dr. Fernando Iñiguez(1), Dr. Ignacio Sánchez(2)
Pediatra Broncopulmonar 1. Hospital Base de Puerto Montt2. Escuela de Medicina. Pontificia Universidad Católica de Chile
Correspondencia: Dr. Fernando Iñiguez Osmer. Pediatra Broncopulmonar.Servicio de Pediatría. Hospital Base de Puerto Montt. Seminario s/n°, PuertoMontt. Teléfono (fono-fax): 56-65490140 E-mail: [email protected]
INTRODUCCIÓN
Muchos eventos que ocurren durante la vida fetal y postnatal
temprana, tienen influencia en la salud respiratoria del niñoy del adulto. El estudio del desarrollo pulmonar constituyeuna atractiva y dinámica área de investigación constante. El
desarrollo alveolar es un fenómeno principalmente postnataly las posibles injurias que afecten al feto o recién nacido (RN)sin duda van a afectar este complejo proceso(1).
Los RN prematuros (RNPT) con frecuencia son sometidos
a terapias como ventilación mecánica a presión positiva yadministración de oxígeno, intentando salvar sus vidas, pero
estas mismas terapias, junto a posibles infecciones respiratoriasasociadas, pueden conducir a daño pulmonar (2).
Con el propósito de comprender la función pulmonar deun RN es necesario conocer el desarrollo normal del pulmón fetal. Para que el RN se adapte al ambiente extrauterino es
necesario que se absorba el fluido pulmonar, que los pulmonesse llenen de aire y que exista una adecuada superficie deintercambio gaseoso(3).
ETAPAS DEL DESARROLLO
El desarrollo pulmonar ocurre como una serie de eventosdinámicos que se relacionan estrechamente entre sí. Paraefectos de su comprensión, se han descrito varias etapas enel desarrollo prenatal del pulmón humano, que se basan ensu morfología (tabla 1). La relación entre el desarrollo de la vía aérea y la vasculatura pulmonar se demuestra en la figura1.
Etapa embrionaria: 3-7 semanas
El brote pulmonar se origina a partir de células epiteliales delendodermo del intestino primitivo anterior, como un divertículo
ventral alrededor del día 24-26 de gestación, que penetrahacia el mesénquima circundante y crece por divisionesdicotómicas en dirección caudal, para formar las estructurasproximales del árbol traqueobronquial. El epitelio de todo elárbol respiratorio, desde las vías aéreas (VA) centrales hastalos neumocitos que recubren los alvéolos, se deriva de estebrote, mientras que el cartílago, músculo liso, tejido conectivoy vasculatura pulmonar tienen su origen en el mesénquima. Alrededor del día 33, ocurre la división en las dos ramasprincipales y los brotes pulmonares yacen a ambos lados del futuro esófago. Al parecer, es el mesoderma circundante elque regula la ramificación del árbol traqueobronquial. Losbronquios lobares inician su formación por el día 37 y hacia

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 8/54
149
Tabla 1.- Etapas del desarrollo pulmonar
FASE EDAD GESTACIONAL PRINCIPALES EVENTOSO POSTNATAL
Embrionaria 3 - 7 semanas Desarrollo de las vías aéreas mayores.
Aparición de circulación pulmonar (vasculogénesis)Pseudoglandular 7 - 17 semanas Desarrollo del árbol bronquial hasta nivel debronquíolos terminales (preacinar).Crecimiento vascular sigue al de la VA.
Canalicular 17 - 27 semanas Formación de acinos.Crecimiento del lecho capilar (angiogénesis)Diferenciación epitelial, aparece el surfactante.
Sacular 28 - 36 semanas Formación de los espacios aéreos transitorios.Depósito fibras elásticas en futuros septos secundarios.
Alveolar 36 semanas - 2 a 3 años Aparición de septos secundarios, formación de alvéolos.
Maduración microvascular 0 - 3 años Adelgazamiento de la pared interalveolar; fusión
de la bicapa capilar a una singular.
Hiperplasia activa 0 - 3 años Aumenta el número de alvéolos, poco cambio en su tamaño.
Hipertrofia 3 - 8 años Aumento del tamaño alveolar, con crecimiento celularmayor al corporal.
Desarrollo pulmonar
el fin de esta etapa (día 42) ya pueden ser reconocidos los19 segmentos pulmonares(2-5).
El mesénquima que rodea los brotes pulmonares contiene
un número de células que se tiñen positivamente para unmarcador de células endoteliales (CD31), indicando así el
origen de los futuros capilares(6). Para el día 34 de gestación,
ya se ha formado una red de capilares alrededor de cada
futuro bronquio principal y este plexo se comunica en dirección
cefálica con el saco aórtico mediante las arterias pulmonares
y hacia caudal con el seno venoso (futura aurícula izquierda)
mediante las venas pulmonares. En este momento ya hay
evidencia de células sanguíneas circulantes(7). Los primeros
vasos pulmonares se formarían entonces “de novo” desde
el mesénquima subyacente por el proceso de vasculogénesis:
diferenciación celular para formar células endoteliales únicas
que se organizan en tubos capilares(4,5)
. Estos capilarescoalescen para formar pequeños vasos sanguíneos a lo largo
de la VA.
Etapa pseudoglandular: 7-17 semanas
En esta etapa se desarrollan las VA principales, a través de
sucesivas divisiones dicotómicas. El nombre de esta etapa
deriva del aspecto glandular en los estudios histológicos, ya
que los bronquiolos terminan en forma ciega en el estroma
primitivo. Desde el mesénquima se desarrollan las células de
la pared bronquial que darán origen al cartílago, músculo liso
bronquial y glándulas submucosas. El número definitivo de
bronquiolos terminales se ha completado al final de esta
etapa. El epitelio columnar seudoestratificado va siendo
reemplazado en forma progresiva por células columnaresaltas en la VA proximal y células cuboidales hacia la periferia(2-4).
En este período, la vasculatura se ramifica siguiendo a la
VA, que actúa como un molde. En la medida que cada nuevo
brote penetra el mesénquima, un nuevo plexo capilar lo
rodea como un halo para unirse luego con los vasos
preexistentes, extendiendo así los vasos arteriales y venosos.
La vasculogénesis continúa hasta la semana 17, al cabo de la
cual todas las VA preacinares y sus respectivas venas y arterias
ya se han formado, con poco mesénquima indiferenciado
remanente entre estas estructuras(4-6)
.
Etapa canalicular: 17-27 semanas
Los bronquiolos terminales se dividen para formar los
bronquiolos respiratorios y ductos alveolares en forma de
sacos, los que constituyen las estructuras acinares. Ocurre
un progresivo adelgazamiento del epitelio, con aproximación
de los capilares los que yacen justo por debajo de este. El
epitelio cuboidal se diferencia y los ductos alveolares están
revestidos de células alveolares (neumocitos) tipo II -las que
darán originen a los neumocitos tipo I- que recubrirán los

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 9/54
Figura 1.- Esquema de la vía aérea con su respectivo epitelio regional.
150Iñiguez F. et al
Vía aérea
1 célula caliciforme
2 célula cilíndrica ciliada3 célula de la membrana basal
4 célula muscular lisa
5 glándula mucosa
6 cartílago
7 capa mucosa superficial
8 célula en cepillo (Brush Cell)
9 célula columnar ciliada
10 capilar
11 célula Clara
12 célula cuboidal ciliada
13 célula epitelial alveolar
(neumocito) tipo 1
14 macrófago alveolar
15 célula epitelial alveolar
(neumocito) tipo 2
16 surfactante
0 - 9 semanasTráquea y Bronquios
10 - 14 semanasBronquíolos
15 - 19 semanas
Bronquiolo respiratorio
19 - 23 semanas Alvéolo
c c e q
sacos distales adelgazándose en la medida que se relacionan
estrechamente con los capilares. Hacia las 24 semanas de
gestación, ya se ha establecido la barrera alveolo-capilar, con
un grosor similar al del adulto (0.2 _m) y el área disponiblepara el intercambio gaseoso permite que algunos prematuros
extremos puedan sobrevivir (5) . Los neumocitos tipo II
aumentan su maquinaria metabólica, preparándose para
sintetizar surfactante y hacia las 24 semanas ya se pueden
observar proteínas del surfactante en la forma de cuerpos
lamelares en su citoplasma. Hacia el final de esta etapa la
periferia del pulmón esta constituida por sáculos transitorios,
de paredes finas, que se han formado gracias a la disminución
en la cantidad de mesénquima(2-5). Los capilares en esta etapa
se forman por angiogénesis (brote de vasos sanguíneos desde
vasos preexistentes) y las células en división se encuentran
en los túbulos capilares más que en el mesénquimaindiferenciado(5,8).
Etapa sacular: 28-36 semanas
En este período continúa la división de la VA periférica. Cada
bronquiolo terminal ha originado 3 generaciones de
bronquiolos respiratorios, cada uno de los cuales origina una
generación de ductos transitorios, los que a su vez generan
3 sáculos que desembocan en los sáculos terminales. De
este modo aumenta el tamaño de la VA periférica y crece la
superficie para el intercambio gaseoso en la medida que la
pared continúa adelgazándose (septos primarios). Por otra
parte, ocurre una preparación para la etapa alveolar al
depositarse fibras elásticas en los puntos donde surgirán los
futuros septos secundarios. Los neumocitos tipo II aumentanel número de cuerpos lamelares y continúa la diferenciación
hacia neumocitos tipo I(2-5). Las arterias que irrigan los ductos
alveolares se desarrollan desde las 25 semanas hasta los 18
meses después del nacimiento. Los alvéolos comienzan a
aparecer después de las 30 semanas y junto a ellos se van
desarrollando los pequeños vasos pre y post capilares(5,8).
Etapa alveolar: 36 semanas a 2-3 años postnatal
El inicio de esta etapa se define por la aparición de pequeñas
prominencias a ambos lados de las paredes saculares, en lospuntos donde se depositaron fibras elásticas. Estas crecen
en forma perpendicular al espacio aéreo, dividiendo los
sáculos en forma incompleta en unidades menores, los
alvéolos, los que también se formarán en menor medida en
bronquíolos respiratorios y en los ductos transitorios. Estos
septos secundarios consisten en una doble asa capilar separada
por una vaina de tejido conectivo.
En este período tiene lugar una marcada proliferación de
todos los tipos celulares . Las células mesenquimáticas
proliferan, depositando la matriz extracelular necesaria y los
neumocitos tipo I y II aumentan su número para delinear las

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 10/54
151
Tabla 2.- Algunos factores de crecimiento (FC) y su rol enel desarrollo pulmonar.
FACTOR ROL
FC transformante ß 1,2
FC epidérmico 2,0
FC de keratinocitos 2,0
FC de fibroblastos 2,3Proteína morfogenética ósea 2,5
FC derivado de plaquetas 3,0
Factor estimulante de coloniasmacrófago-granulocito
4,7
FC del endotelio vascular 5,0
FC insulino-símil 6,0
Rol más importante de algunos FC sobre el desarrollo pulmonarembrionario y postnatal. 1 = Producción de matriz extracelular; 2 =Ramificación, crecimiento y diferenciación del epitelio de la vía aérea;3 = Desarrollo alveolar; 4 = Diferenciación de los macrófagos; 5 =Neovascularización; 6 = Ramificación temprana del epitelio de la víaaérea; 7 = Catabolismo del surfactante.
Desarrollo pulmonar
paredes alveolares, donde aproximadamente un 85-90%
de la superficie estará recubierta de neumocitos tipo I (2,3).
En la medida que se forman nuevos alvéolos, también se
forman nuevos capilares por angiogénesis. Por otra parte,
se incrementa el tamaño de las venas y arterias proximales,
acomodando así el aumento de flujo y volumen sanguíneo
al lecho capilar en crecimiento(5,7). Los procesos mencionados
tienen como resultado un aumento en la superfi cie de
intercambio gaseoso y una preparación de las células de la
VA que responderán al ambiente extrauterino (2).
DESARROLLO DE LA CIRCULACIÓN BRONQUIAL
El segundo sistema circulatorio del pulmón humano es la
circulación bronquial, mediante la cual se suministra oxígeno
y nutrientes a las paredes de la VA y grandes vasos pulmonares.
En adultos, las arterias bronquiales alcanzan hasta la periferia
de los ductos alveolares.
Su formación no es simultánea con la circulación pulmonar,
ya que se inicia alrededor de las 8 semanas con el nacimiento
de uno o dos vasos que nacen de la aorta dorsal y se dirigen
hacia el pulmón, relacionándose con las placas cartilaginosas
de los bronquios fuentes y extendiéndose luego hacia la
periferia, en la medida que las VA crecen y se diferencian los
componentes de sus paredes. Estos vasos forman una red
a través de la pared de la VA, tanto bajo el epitelio como en
la pared externa, con un tamaño pequeño si se les compara
con los vasos pulmonares cercanos. Varias venas bronquiales
pequeñas de la VA drenan en las venas pulmonares, mientrasque las venas bronquiales de mayor tamaño en el hilio drenan
en las venas cardinales y aurícula derecha ( 4 ,5 ).
CRECIMIENTO POSTNATAL
El gran desarrollo del parénquima pulmonar ocurre después
del nacimiento. La formación de alvéolos ocurre
aceleradamente en los primeros meses de la vida, sobre todo
en los dos primeros, con maduración de los ductos
transicionales y sáculos alveolares. La fase alveolar se prolonga
hasta los 2-3 años, con aumento del número más que del
tamaño de los alvéolos(2-4).
En los septos secundarios, las células epiteliales experimentan
un masivo crecimiento, seguido de fenómenos de apoptosis
(muerte celular programada sin inflamación) que remodelan
la irrigación del septo, desde un asa capilar doble hacia la
morfología definitiva con un asa capilar única, proceso conocido
como maduración microvascular. Este fenómeno se inicia al
nacer y se prolonga hasta los 3 años aproximadamente(2,4,9).
Entre los 3 y 8 años, ocurre crecimiento pulmonar por
aumento del número y también del tamaño de los alvéolos.
Posteriormente, el crecimiento del pulmón es acorde con
el del resto del organismo hasta los 18 años. Se estima que
al nacer el número de alvéolos es de 20-50 millones. Hacia
los 8 años este número ha alcanzado unos 300 millones,
muy semejante al del adulto. En cuanto a la superficie de
intercambio gaseoso, se estima que esta corresponde a
unos 2,8 mt2 al nacer, 32 mt 2 hacia los 8 años y 75 mt 2
en la adultez(2,9,10).
MECÁNICA RESPIRATORIA
Se estima que la capacidad residual funcional (CRF) es alrededor
de 21 mL/Kg en RN de término de ambos sexos (11) y la
distensibilidad (compliance) total del sistema respiratorio (Crs)
de 5 mL/cmH2O, dada fundamentalmente por el pulmón,
ya que la pared torácica a esta edad es muy distensible o
complaciente.
Esto difiere de la situación del adulto, donde la distensibilidad
del pulmón y de la pared torácica es muy similar. La resistencia
total del sistema respiratorio está cercana a 70 cmH2O/L/seg,
la mayor parte de la cual está en el árbol bronquial. Se estima
que la distensibilidad del RN es 1/12 de la del adulto y la
resistencia 15 veces mayor (9). En la primera respiración se
puede generar una presión intra torácica cercana a -70
cmH2O(10).
El volumen corriente de un RN de término es 6-8 ml/Kg.
y el volumen minuto es cercano a 0.6 litros. El espacio muerto
anatómico se aproxima a la mitad del volumen corriente, lo
que se traduce en una ventilación alveolar de 0,3 l/min. El
consumo de oxígeno está en el rango de 20-30 mL/min.(10,12).

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 11/54
152
Figura 2.- Factores pre y postnatales que influyen sobre el desarrollo pulmonar
Los factores nutricionales y hormonales actúan tanto en el período prenatal como en el postnatal. El factor infección también puedeactuar de modo prenatal. adaptado de ref. 2 (DAP: di¡uctus arterioso persistente. O2: oxígeno. VA: vía área. VM: ventilación mecánica).
Anomalías
del desarrolloContraciones
paristálticas de la V A
CRECIMIENTOPULMONAR
Bienestar
materno - fetalCarga genética
Movimientosrespiratorios
Tabaquismo pasivo
Toxicidad O2
Biotrauma por VMEnfermedad por
déficit de surfactante
DAPInfección
Hormonal
Nutricional
Prematurez
PR E
N A T A L
POSTN A T A L
Iñiguez F. et al
ÍNDICE PESO PULMONAR/PESO CORPORAL
La evaluación del desarrollo pulmonar es un componente
muy importante en el caso de una autopsia perinatal. Uno
de los elementos a considerar es el índice peso pulmonar/peso
corporal. Se han publicado recientemente valores de referenciaen población de Estados Unidos(13).
Este índice permanece más o menos estable entre las 17-27
semanas, con una media cercana a 3%, para disminuir a
medida que la gestación progresa, siendo la media en RN
de término 1,79%. Puede resultar útil la comparación con
el percentil 10 en caso de sospecha de hipoplasia pulmonar.
Este valor es cercano a 2.2% entre las 16-23 semanas, 2.59%
entre las 24-27 semanas, 2.27% entre las 28-36 semanas y
1.24% entre las 37-41 semanas. La comparación con el
percentil 10 puede detectar grados más leves de hipoplasia
pulmonar que los tradicionales valores propuestos por
Wigglesworth(14) en 1981, de 1.2% como el límite inferiorde la normalidad para RNPT de más de 28 semanas y de
1.5% para los menores de esa edad gestacional.
CONTROL GENÉTICO DEL DESARROLLOPULMONAR
El desarrollo pulmonar constituye un proceso altamente
organizado, en el cual las interacciones del mesénquima con
el epitelio controlan y coordinan la expresión temporal y
espacial de múltiples factores regulatorios, los que son
necesarios para la adecuada formación y crecimiento del
pulmón. Diversos factores tanto endógenos como exógenos
pueden alterar este delicado equilibrio, lo que conduce a
desordenes en el crecimiento, maduración o función de los
tejidos en formación(15). Para cada una de las etapas del
desarrollo pulmonar, se han identificado una serie de factores
controladores, principalmente factores de transcripción y de
crecimiento (junto a sus respectivos receptores), moléculas
de la matriz extracelular, integrinas y moléculas de adhesión
intercelular, entre otras. En su conjunto, estos factores
interactúan a lo largo del eje proximal-distal del sistema
respiratorio, influenciando localmente múltiples genes, que
en definitiva controlan el modelamiento del endodermo y la
morfogénesis de las ramificaciones pulmonares, la asimetría
derecha-izquierda, la vascularización y la respuesta a las fuerzas
mecánicas(2,16).
Los factores de crecimiento (FC) son proteínas difusibles
que actúan a corta distancia desde su sitio de producción,induciendo variadas actividades celulares por medio de
intricadas señales bioquímicas. No solo promueven la
proliferación celular, sino también son importantes mediadores
de interacciones titulares, tanto durante la embriogénesis
pulmonar así como también en la vida postnatal. En la
organogénesis, estas moléculas proveen información para las
adecuadas respuestas de retroalimentación entre las diferentes
capas germinales. Los FC definen los centros de señales
celulares que controlan el comportamiento de las células
vecinas, al formar gradientes en una estructura en desarrollo.
En el pulmón en desarrollo, los FC definen patrones de

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 12/54
153
Tabla 3.- Etapas del desarrollo pulmonar en que se generanciertas malformaciones congénitas, asociadas a desarrollopulmonar anómalo.
1. Embrionario
Agenesia pulmonar, laríngea o traqueal
Estenosis laríngea o traquealTraqueomalacia y broncomalacia
Malformaciones bronquiales
Pulmón en herradura
Malformaciones arterio-venosas
Quistes pulmonares congénitos (incluye Q. broncogénico)
Fístula traqueoesofágica
2. Pseudoglandular
Malformación adenomatoídea quística
Hipoplasia pulmonar
Quistes pulmonares
Linfangectasia pulmonar congénita
Hernia diafragmática congénita
Secuestro pulmonar
3. Canalicular
Hipoplasia pulmonar
Displasia acinar
4. Sacular-alveolar
Hipoplasia pulmonar
Displasia acinar
Displasia alveolo-capilar
Desarrollo pulmonar
ramificación y controlan el tamaño de la VA y el destino celular,
entre otras funciones. En general, los FC que ejercen su señal
mediados por receptores del tipo tirosina-kinasa promueven
la diferenciación y multiplicación celular (ej. FC de fibroblastos,
FC epidérmico, FC vascular endotelial, FC derivado de las
plaquetas). Se oponen a estos efectos los FC que actúan a
través de receptores del tipo serina-treonina kinasa (ej. FC
transformante 1, proteína morfogenética ósea 4). Estas señales
logran un delicado equilibrio cuando el pulmón ya está
desarrollado, de modo de preservar las actividades celulares
y la estructura y función pulmonar (17). La tabla 2 incluyealgunos FC y su función en diferentes etapas del desarrollo (15-
22).
FACTORES QUE INFLUYEN SOBRE EL DESARROLLOPULMONAR
Para que exista un normal desarrollo pulmonar, es fundamental
la presencia de movimientos respiratorios fetales (MRF), un
adecuado espacio intratorácico, fluido intra y extrapulmonar
en volumen suficiente y una adecuada irrigación. La salud
materna en aspectos tales como nutrición, factores endocrinos,
consumo de tabaco y morbilidades -tanto relacionadas con
el embarazo (diabetes gestacional, síndrome hipertensivo)
como no relacionadas con él- también influyen sobre el
desarrollo del feto (figura 2).
Anomalías del desarrolloEn cualquiera de las etapas del desarrollo pulmonar descritas,
pueden ocurrir anormalidades debidas a factores materno-
fetales (ej. oligohidroamnios), genéticos (ej. déficit de proteína
B del surfactante) o anomalías del desarrollo. La tabla 3 ilustra
algunas de estas condiciones, según la etapa en que ocurren(2,3). La tabla 4 enumera los factores que influyen de modo
adverso en el desarrollo pulmonar, tanto en el período
prenatal como postnatal(23,24).
Respiración fetal y fluido pulmonar El fluido pulmonar es producido por las células epiteliales del
pulmón, sobre todo por aquellas de la VA distal y fluye hacia
el líquido amniótico (LA) o es deglutido. Este fluido es pobre
en proteínas y bicarbonato y rico en cloro; su velocidad de
producción aumenta a medida que la gestación progresa. Su
presencia en la VA establece una ligera presión positiva con
respecto a la existente en el LA y previene el colapso. Hacia
el final de la gestación la vía aérea del feto contiene
aproximadamente 40 ml, de rápido recambio. Es el balance
entre la producción y el drenaje lo que parece crucial en el
desarrollo del pulmón(3,25).
Se han detectado MRF desde las 11 semanas y hacia el
final de la gestación estan presentes durante la tercera parte
del tiempo, aumentando en los períodos de actividad fetal,
siendo el diafragma el principal músculo involucrado. Existe
un ritmo circadiano de los MRF, con disminución de ellos en
las horas previas a la medianoche y aumento entre las 4 y 7
AM. Los MRF aumentan tras la alimentación materna
(hiperglicemia), al igual que en situaciones de hipercapnia,
acidosis, aumento de la temperatura y ante administración
de indometacina, cafeína y teofilina. Una depresión en los
MRF se observa en condiciones de hipoxia (depresor global
de la actividad fetal), hipoglicemia, infección intrauterina oconsumo materno de tabaco, alcohol o sedantes como el
diazepam y la morfina(3). Los MRF son fundamentales porque
permiten mantener un adecuado volumen pulmonar. En los
períodos de apnea, la faringe está colapsada y la laringe ofrece
resistencia a la salida del líquido, con mantención de la gradiente
de presión. En la fase inspiratoria, la VA superior se dilata y
el diafragma se contrae, permitiendo la entrada del líquido,
lo que contribuye a la expansión pulmonar (26) .
Hacia el final de la gestación, el volumen del fluido pulmonar
y su velocidad de producción disminuyen. Estos cambios
ocurren en una etapa del desarrollo pulmonar en que se

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 13/54
154
Tabla 4.- Factores que afectan de modo adverso el desarrollopulmonar.
I. Prenatal
A.- Reducción del espacio intratorácico:
Alteraciones del diafragma:- Agenesia diafragmática- Hernia posterolateral o de Bochdaleck - Hernia anterior o de Morgagni- Eventración
Malformación adenomatoídea quística:- Tipo 0: displasia acinar - Tipo I: múltiples quistes grandes o uno dominante- Tipo II: múltiples quistes pequeños- Tipo III: masa sólida- Tipo IV: quistes periféricos
Secuestro pulmonar:- Intralobar - Extralobar
Enfisema lobar congénito
Derrame pleural:- Idiopático- Quilotórax- Asociado con anomalías cromosómicas, cardiopatía
congénita, hernia diafragmática congénita.- Hidrops generalizado: inmunológico y
no inmunólogico
Desórdenes esqueléticos:- Distrofia asfixiante torácica (Síndrome de Jeunne)- Síndrome de Ellis and van Creveld- Síndrome de Saldino y Noonan (Síndrome de
costillas cortas tipo I)
- Síndrome de Majewski (Síndrome de costillascortas tipo II)- Displasia diastrófica- Dwarfismo tanatofórico- Osteogénsis imperfecta- Acondrogénesis- Hipofosfatasia- Displasia campomélica- Sindrome de Jarcho-Levine
Disminución de los movimientos respiratorios fetales:- Anomalías neurológicas: Sindrome de
Werdnig-Hoffmann, distrofias musculares congénitas- Defectos de la pared abdominal anterior:
onfalocele, gastrosquisis- Drogas: tabaco
B.- Reducción del volumen de líquido amniótico:(oligohidroamnios)
- Producción disminuida: nefropatías (ej. Potter)- Pérdida de líquido amniótico (rotura prematura
de membranas)- Procedimientos invasivos: amniocentésis
II. Postnatal
Prematurez
Drogas:- Humo de tabaco ambiental- Corticoides
Iñiguez F. et al
incrementa la expresión en el epitelio de los canales de sodio
y la bomba sodio-potasio ATPasa. Estos cambios en el
transporte de iones en las células epiteliales pulmonares en
la gestación tardía, reflejan el cambio desde un patrón de
secreción de cloro a uno de absorción de sodio cerca del
nacimiento, preparando así al pulmón para su adaptación
postnatal(27).
Contracciones peristálticas
Estudios en animales han destacado la importancia de las
contracciones peristálticas espontáneas que ocurren en la VA(21). Estas ondas peristálticas se originan en la tráquea y se
propagan por el árbol bronquial, con lo que impulsan el
líquido pulmonar hacia distal. Al relajarse los túbulos, el flujo
se revierte. En pulmones fetales de cerdos en etapas
pseudoglandular y canalicular, la frecuencia es de 2-3/min,
mientras que en pulmones de conejo en etapa sacular es de10-12/min. La presión intraluminal medida en la traquea del
feto de conejo es 2.3 cmH2O. Es muy probable que la
expansión de los brotes más periféricos se vea favorecida
por este fenómeno, al facilitar su crecimiento hacia el
mesénquima circundante(28).
Corticoides
La administración prenatal de corticoides acelera el crecimiento
pulmonar por variados mecanismos. Entre ellos, favorecen
la maduración del pulmón con incremento en la densidad
volumétrica de los espacios aéreos junto con un aumentoen la maduración del epitelio pulmonar. Se promueve un
adelgazamiento precoz de la doble asa capilar durante las
etapas sacular y alveolar, pero disminuye el número final de
septos secundarios y con ello el número final de alvéolos.
Los neumocitos tipo II aumentan en número, además de
desarrollarse funcionalmente, con aumento en los niveles de
ARN mensajero para las proteínas del surfactante. Otros
efectos incluyen el aumento en la transcripción de genes
responsables del crecimiento y la maduración, además del
incremento en los niveles de enzimas antioxidantes.
Administrados en forma postnatal, los corticoides aceleran la
maduración del tejido pulmonar en desarrollo, acortando el
tiempo en el que se encuentra presente la doble asa capilar
que es vital para el desarrollo de los septos secundarios. De
este modo, se acorta la septación y se limita el número total
de alvéolos que pueden desarrollarse(29).
Por otra parte, los corticoides antenatales (CA), cuando
hay amenaza de parto prematuro, van a afectar la mecánica
respiratoria. Un estudio prospectivo reciente(30) comparó la
compliance del sistema respiratorio (Crs) de RNPT ( 32
semanas de gestación, < 3 días de vida, previo a administrar
surfactante si se requería) que recibieron los CA más de una

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 14/54
REFERENCIAS1. Bush A. Update in pediatric lung disease 2007. Am J Respir Crit Care Med 2008;
177: 686-95.2. Kotecha S. Lung growth: implications for the newborn infant. Arch Dis Child Fetal
Neonatal Ed 2000; 82: 69-74.3. Kotecha S. Lung growth for beginners. Pediatr Respir Rev 2000; 1: 308-13.4. Hislop A. Airway and blood vessel interaction during lung development. J Anat
2002; 201: 325-34.5. Hislop A. Developmental biology of the pulmonary circulation. Pediatr Respir Rev
2005; 6: 35-43.6. Hall S., Hislop A., Pierce C., Haworth S. Prenatal origins of human intrapulmonary
arteries: formation and smoth muscle maturation. Am J Resp Cell Mol Biol 2000;23:194-203.
7. Hall S., Hislop A., Haworth S. Origin, differentiation and maturation of humanpulmonary veins. Am J Resp Cell Mol Biol 2002; 26:333-40.
8. Hislop A., Pierce C. Growth of the vascular tree. Pediatr Respir Rev 2000; 1: 321-27.
9. Sánchez I. Desarrollo del aparato respiratorio y diferencias anatómicas y funcionalesentre el lactante y el adulto. Pediatr ía al Día 2001; 17: 251-4.
10. Pregnancy, neonates and children. En: Lumb AB, ed. Nunn's Applied RespiratoryPhys io logy, 5ª ed. Ed inburgo, But terworth Heinemann, 2000.
11. Hulskamp G., Pillow J., Dinger J., Stocks J. Lung function tests in neonates andinfants with chronic lung disease of infancy: functional residual capacity. PediatrPulmonol 2006; 41: 1-22.
12. Tapia J., Toso P., Bancalari E. Enfermedades respiratorias de l recién nacido. En:Sánchez I., Prado F., ed. Enfoque Clínico de las Enfermedades Respiratorias delNiño. Ediciones Universidad Católica de Chile, 2007.
13. De Paepe M., Friedman R., Gundogan F., Pinar H. Postmortem lung weight/body weight standards for term and preterm infants. Pediatr Pulmonol 2005; 40: 445-8.
14. Wigglesworth J., Desai R. Use of DNA estimation for growth assessment in normaland hypoplastic fetal lungs. Arch Dis Child 1981; 56: 601-5.
15. Roth-Kleiner M., Post M. Genetic control of lung development. Biol Neonate2003; 84: 83-8.
16. Copland I., Post M. Lung development and fetal lung growth. Pediatr Respir Rev2004;5 (Suppl A): S259-S264.
17. Desai T., Cardoso W. Groth factors in lung development and disease: friends or foe? Respir Res 2002; 3: 2. Epub 2001 Oct 9.
18. Ware L., Matthay M. Keratinocyte and hepatocyte growth factors in the lung: rolesin lung development, inflammation, and repair. Am J Physiol Lung Cell Mol Physiol2002; 282: L924-L940.
19. Bartram U., Speer C. The role of transforming growth factor ≤ in lung developmentand disease. Chest 2004; 125: 754-65.
20. Naito M. Macrophage differentiation and function in health and disease. Pathol Int2008; 58: 143-55.
21. Le Souëf P. Growth and development of the lung. Curr Opin Allergy Clin Immunol
2001; 1: 127-31.22. Roth-Kleiner M., Post M. Similarities and dissimilarities of branching and septation
during lung development. Pediatr Pulmonol 2005; 40: 113-34.23. Greenough A. Factors adversely affecting lung growth. Pediatr Respir Rev 2000;
1: 314-20.24. Girosi D., Bellodi S., Sabatini F., Rossi G. The lung and the gut: common origins,
close links. Pediatr Respir Rev 2006; 7S: S235-S239.25. Wilson S., Olven R., Walters D. Developmental regulation of lumenal lung fluid
and electrolyte transport. Respir Physiol Neurobiol 2007; 159 :247-55.26. Miller A., Hooper S., Harding R. Role of fetal breathing movements in control of
fetal lung distension. J Appl Physiol 1993; 75: 2711-17.27. Bland R. Loss of liquid from the lung lumen in labor: more than a simple "squeeze".
Am J Physiol Lung Cell Mol Physiol 2001: 280: L602-5.28. Schittny J., Miserocchi G., Sparrow M.. Spontaneous peristaltic airway contractions
propel lung liquid through the bronchial tree of intact and fetal lung explants. Am J Respir Cell Mol Biol 2000; 23: 11-18.
29. Gibson A. Perinatal corticosteroids and the developing lung. Pediatr Respir Rev2002; 3: 70-76.
30. McEvoy C., Schilling D., Spitale P., Peters D., O'Malley J., Durand M. Decreased
respiratory compliance in infants less than or equal to 32 weeks' gestation, deliveredmore than 7 days after antenatal steroid therapy. Pediatrics 2008; 121: e1032-e1038.
31. Lopuhaa C., Roseboom T., Osmond C, et al. Atopy, lung function, and obstructiveairways disease after prenatal exposure to famine. Thorax 2000; 55:555-61.
32. American Thoracic Society Documents. Mechanisms and limits of induced postnatallung growth. Am J Respir Crit Care Med 2004; 170: 319-43.
155 Desarrollo pulmonar
semana antes de nacer, con aquellos que los recibieron 1-7
días antes del parto.
La Crs se midió con la técnica de oclusión en respiración
única, con 28 pacientes en cada grupo. Los niños nacidos
después de una semana de administrados los CA tuvieron
valores significativamente menores de Crs, tanto en el valorabsoluto como al normalizar por peso, al comparar con
aquellos que nacieron entre 1-7 días después de administrado
el medicamento (1.52 mL/cmH2O versus 2.12 mL/cmH2O
y 0.98 mL/cmH2O/Kg versus 1.41 mL/cmH2O/Kg). Los
autores especulan que la menor Crs puede reflejar la disipación
del efecto benéfico sobre la función pulmonar de los CA
cuando el parto ocurre después de 7 días de recibida la
terapia.
Nutrición
La malnutrición fetal parece disminuir los volúmenes
pulmonares pero no la maduración de las vías aéreas. Estudios
en animales muestran que la disminución en la nutrición fetal
altera el proceso de desarrollo de los septos secundarios,
con disminución del área de intercambio, sin afectarse el
tamaño final del alveolo(2). Se postula que ocurre menor
depósito de elastina en las fases sacular y alveolar. Este hecho,
sumado a que en el lactante desnutrido existe menos masa
muscular, aumenta la tendencia al colapso bronquiolar durante
las infecciones respiratorias. Estudios realizados en adultos,
hijos de madres que sufrieron hambruna en el período 1944-
1945, realzan la importancia de la adecuada nutriciónintrauterina sobre el desarrollo pulmonar. Aquellos sujetos
expuestos a malnutrición materna durante el segundo o tercer
trimestre de la gestación tenían una incidencia mayor de
enfermedades obstructivas de la VA en la adultez, sin alteración
en el nivel de Ig E ni en las pruebas de función pulmonar (31).
CONCLUSIONES
El desarrollo pulmonar es un proceso altamente coordinado
y complejo, sobre el que aun falta mucho por conocer. En
el ser humano, este proceso es especialmente intrincado, al
nacer con solo una parte de los alvéolos que se tendrán enla vida adulta, ya que el desarrollo alveolar es fundamental-
mente postnatal. Los avances futuros quizás nos entreguen
herramientas concretas para poder ayudar a los RN aquejados
de displasia broncopulmonar o de otras condiciones congénitas
en que se alteró el normal desarrollo pulmonar (32).
AGRADECIMIENTOS
El autor agradece al Dr. Luis E. Vega-Briceño por sus consejos
y constante aliento para la confección de este artículo.

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 15/54
Resumen
El uso de ecuaciones de referencia adecuadas para determinar y predecir valores normales es unaspecto importante para optimizar la utilidad clínica de las pruebas de función pulmonar. Debido ala diversidad de ecuaciones existentes, cada laboratorio de función pumonar debe saber elegir lasapropiadas para su población de estudio. Estas ecuaciones deberían ser consistentes y representativas,deberían derivar de estudios que utilicen procedimientos y equipos estandarizados y por supuesto,deberían estar validadas. Existen muchos factores determinantes de la función pulmonar en un niñoo adolescente, como son: la estatura, sexo y edad; y recientemente se ha publicado evidencia quesugiere el rol de la influencia racial, ambiental y de los potenciales efectos de la pubertad. En esta
revision se brinda una revision de estos factores y de su efecto en la determinacion de volumnespulmonares en niños escolares y adolescente.
Palabras Claves: volúmenes pulmonares, pletismografía, factores, niños, adolescentes.
NEUMOLOGIA PEDIATRICA ISSN 0718-3321
Determinación de valores de referencia para volumenes pulmonares en escolares y adolescentesDra. Solange Caussade
Pediatra Broncopulmonar Departamento de PediatríaPontificia Universidad Católica de Chile
Correspondencia: Dra. Solange Caussade Pediatra Broncopulmonar.Departamento de Pediatría. Pontifícia Universidad Católica de Chile. Email:[email protected]
156
VRI: Volumen de Reserva Inspiratoria: volumen máximo inspirado luegode una inspiración a volumen corriente.
VC: Volumen Corriente: volumen de gas inhalado o exhalado durantela respiración de reposo.
VRE: Volumen de Reserva Espiratoria: volumen máximo de gas exhaladoluego del final de una espiración de reposo.
CV: Capacidad Vital: es el volúmen medido luego de una inspiraciónmáxima seguida de una espiración máxima.
VR: Volumen Residual: volumen de gas restante en e l pulmón luegode ulna espiración forzada.
CI: Capacidad Inspiratoria: volumen máximo de gas inspirado a partir de CRF.
CRF: Capacidad Residual Funcional: volumen de gas presente en elpulmón luego del final de una espiración de reposo.
CPT:Capacidad Pulmonar Total: es la suma de todos los volúmenes.
VRI
VC
VRE
CV
VR
CI
CRF
CPT
Figura 1.- Volúmenes y capacidades pulmonares estáticos
disponible en http://www.neumologia-pediatrica.cl
INTRODUCCIÓN
La medición de volúmenes pulmonares es una herramientaútil para detectar, caracterizar y cuantificar la severidad dediversas enfermedades pulmonares. En pediatría, sus principalesindicaciones son la evaluación de pacientes con enfermedad
obstructiva crónica (fibrosis quística, bronquiolitis obliterante,etc), enfermedad restrictiva (enfermedad intersticial crónicade diversas etiologías, enfermedades de la caja torácica, etc)y pacientes que muestran una capacidad vital forzada disminuidaen una maniobra con espirometría.
Las técnicas actualmente utilizadas para determinar volúmenes pulmonares totales son: pletismografía corporal(considerada como gold standard), lavado de nitrógeno,dilución de gas (Helio) y métodos imagenológicos. La Figura1 muestran los volúmenes y capacidades pulmonares posiblesde medir.
Los valores de referencia utilizados para interpretar un
resultado, tienen un rol fundamental para establecer si losresultados obtenidos por el paciente estan en rango denormalidad o si deben considerarse alterados. Para esto, lospatrones de referencia deben ser consistentes, provenir depoblación sana representativa -acorde a las características delpaciente- y deben haber sido obtenidos por el mismo métodode medición. Al elegir ecuaciones predictivas debieran tomarseen cuenta diversos factores, que serán discutidos a continua-ción, lo que permitirá optimizar decisiones clìnicas en relación
a cada paciente en particular. A la fecha, la sociedad americanade torax (ATS) y la sociedad europea de respiratorio (ERS),sugieren utilizar los valores predictivos de Cook y Hamann

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 16/54
157 Determinación de valores de referencia para volumenes pulmonares en escolares y adolescentes
Figura 2.- Medición de volumenes pulmonares en un niñoescolar mediante pletismógrafo
Laboratorio respiratorio pediátrico. Pontificia Universidad Católica de Chile.
para métodos de dilución, y Zapletal y colaboradores para
pletismografía; ambos derivados de escolares y adolescentes
caucásicos(1,2).
FACTORES CONDICIONANTES DE LA PRECISIÓN
DE VALORES PREDICTIVOS DE FUNCIÓN PULMONAREN NIÑOS
Talla
En relación a los volúmenes pulmonares, la talla es la variablepredictiva más potente(2-4). Durante la edad pre-escolar y
escolar, la relación entre talla y volúmenes pulmonares muestra
una relación lineal. Posteriormente en la adolescencia elcrecimiento pulmonar se ve retrasado luego del rápido
aumento de la talla que ocurre durante el “estirón” puberal,y por ello se observa un cambio en la relación entre volumen
pulmonar y talla durante este período(2). Este aspecto se
presentará en la sección siguiente.
En pacientes con enfermedades que disminuyen la talla
tales como la cifoescoliosis o en aquellos que no logranbipedestación, tales como pacientes con alguna enfermedad
neuromuscular , debe sustituirse ésta por la envergadura(2,5,6). Algunos investigadores sugieren medir la talla sentado en vez
de pie, para evitar problemas con las ecuaciones predictivasa utilizar en diferentes razas(5,7,8), otros sostienen que el uso
de la talla sentado no resuelve el problema de las diferencias
raciales(2). Se debe considerar que la medición de la talla
sentado está sujeta a mayores errores que la medición de la
talla en bipedestación o de pie(9).
Edad
En pediatria, debido a la amplia variación en los patrones de
crecimiento, la mayoría de las ecuaciones de regresión no
incluyen la edad como factor predictivo, sino sólo la talla. Si
se agregaran la edad y el peso; el intervalo de confianza de
estas ecuaciones no siempre se estrecha (Figura 2).
En el grupo de edad entre 15 y 20 años se debe ser
cauteloso al momento de utilizar valores predictivos ya que
los estudios pediátricos habitualmente incluyen sujetos hasta
los 15 años y los estudios hechos en población adulta sebasan en un número escaso de sujetos entre 15 y 18 años.
Si en este grupo consideramos por ejemplo, un sujeto
hombre de 18 años y uno de 70 años, ambos de 1,75 cm
de talla, los valores de función pulmonar teóricos serán iguales;
sin embargo, los valores obtenidos por el sujeto joven serán
superiores a los obtenidos en el adulto mayor, subestimándose
los valores teóricos del primero(5).
La evolución de la función pulmonar varía según el estadío
de desarrollo del niño, incrementandose de manera lineal
con la edad hasta la aparición del “estirón” puberal aproxima-
damente a los 10 años en las niñas y 12 años en los varo-
nes(2,10). El crecimiento pulmonar se retrasa en relación a laestatura durante este período, observándose luego un peakalrededor de 18 meses posterior al “estirón” puberal.
Este crecimiento pulmonar acelerado se ha observadoespecialmente en los varones; la altura del tórax aumenta en forma desproporcionada a la talla total y a diferencia de las
mujeres, el tamaño del tórax en los hombres tambien aumentaen su ancho(1,11,12).
Peso
La mayoría de estudios no considera el peso como factorpredictor (5,13) . Se ha visto que la CRF y el VRE, se correlacionaninversamente con el peso y en los casos de obesidad seobserva disminución de CPT y CV (5); FRC y VRE(14).
Género
En general a partir de la edad escolar se observa diferenciaen los valores de función pulmonar según el género, siendosuperiores en los niños. Esto se debería a diferencias en el tamaño y configuración de la caja torácica y a diferencias enla fuerza muscular respiratoria(5).
En las niñas no se ha encontrado discontinuidad duranteel período puberal, mientras que en los varones se ha vistoun incremento importante de la función pulmonar en aquelloscon talla entre 162,6 y 175,5 cms. quienes progresaban deestadio 3 a 4 de Tanner (12).
Raza
La raza negra presenta volúmenes pulmonares inferiores alos individuos de raza blanca, pudiendo alcanzar diferenciasde hasta 23%(5). Los orientales e indios también muestrancifras inferiores a los blancos(15). Si no se cuenta con valorespropios, se sugiere utilizar un factor de corrección(5).

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 17/54
158Caussade S.
La magnitud de estas diferencias no ha sido bien definida
ya que se ha visto que estas son menores en asiáticos que
se han crecido en un ambiente y dieta occidental(2). La ATS
sugiere no realizar correciones para TLC y VR en hispanos
o nativos americanos que viven en USA, pero sí para ameri-
canos africanos, asiáticos e indios(2).
No existe aún una explicación para estas diferencias raciales,
pudiendo tratarse de factores como forma y altura de la caja
torácica, mayor masa pulmonar (mayor número o tamaño
alveolar), diferente relación tronco:extremidades, diferencias
en la proporción masa muscular/grasa, fuerza muscular
respiratoria(1,2,15-18).
Tabaquismo
Al elaborar ecuaciones de referencia en adultos no fumadores,
exfumadores y fumadores actuales, se observó que existía
diferencia significativa entre ellas(19). Con respecto al tabaquismo
pasivo, se vió que la disminución en la función pulmonar no
era significativa(19). Se sugiere seleccionar sujetos no sometidos
a tabaquismo activo para definir valores normales de función
pumonar en niños o adolescentes(5).
Altitud
No se ha encontrado diferencia entre individuos que viven
a nivel del mar y a 1400 metros sobre el nivel del mar. Sin
embargo, estas diferencias si aparecen al vivir en una altitud
superior a los 3000 m.s.n.m(5). Existen estudios realizados
en ciudades de la cordillera de los Andes que muestran quelos niños originarios de baja altitud, al migrar a grandes alturas
precozmente durante su vida, o que han nacido y crecido
en esta situación muestran valores de función pulmonar
significativamente mayores que los niños que han nacido y
crecido a bajas altitudes(20).
SELECCIÓN DE ECUACIONES ADECUADAS
Para asegurarnos una correcta interpretación de resultados,
debemos tomar en cuenta los siguientes aspectos de las
ecuaciones elegidas.
Sujetos elegidos para muestras de referencia
- De preferencia selección de sujetos al azar , y no voluta-
rios.
- Muestra > 200 sujetos.
- Número adecuado de sujetos en edades pediátricas
extremas.
- Raza acorde al paciente en estudio.
- Definición de sano(1): libre de enfermedad respiratoria
aguda ni crónica, sin anomalía congénita, sin antecedente
de neumonia ni cirugía torácica, sin enfermedad crónica
de ningún sistema, sin historia de infección respiratoriaalta las 3 semanas previas al examen.
- No fumadores activos.
- Estado nutricional representativo de la población.
De la técnica
- Técnicos validados.
- Mediciones reproducibles.
- Técnica y equipo semejantes.
De los valores de referencia a utilizar
- Todos los parámetros a utilizar deben provenir de la
misma fuente.
- Si no corresponden a la raza, deben ajustarse.
- Evitar el uso de ecuaciones que no incluyan el rango de
edad ni talla del sujeto que realiza medición de su función
pulmonar.
- Las ecuaciones deben ser diferentes para hombres y
mujeres.
- Para cada ecuación de referencia debiera existir la
definición del valor mínimo y máximo. L os valores
inferiores al percentil 5, se consideran bajo el rango
“normal”. En pediatría puede aceptarse utilizar el valor
de un 80% del predictivo, pero en adultos puedeconducir a errores de interpretación(2).
SITUACIÓN EN CHILE
En Chile existen algunos laboratorios de función pulmonar
que cuentan con pletismógrafo corporal, otros con equipo
para realizar lavado de nitrógeno. La medición de volúmenes
pulmonares mediante pletismografía puede ser realizada sin
dificultad en niños desde los 7 años y es considerada como
el gold standard. Si bien existe un estudio nacional, utilizando
el método de lavado de nitógeno, éste incluyó sólo niños
entre 4 y 13 años(21). El estudio de Díaz y colaboradores
demostró una buena correlación con la estatura del niño.
Por otra parte, un estudio publicado por Gutiérrez y
colaboradores (22) realizado en población sana residente en
las ciudades de Viña del Mar y Valparaíso, encontró que las
variables espirométricas eran significativamente superiores a
las reportadas por Knudson(23) utilizadas como referencia.
CONCLUSIÓN
Debido al número creciente de niños con enfermedad o
daño pulmonar crónico en nuestro medio, es fundamental
contar con ecuaciones de referencia propias para la determi-

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 18/54
REFERENCIAS
1. Stocks J, Quanjer Ph.H. Workshop report. Reference values for residual volume, functional residual capacity and total lung capacity. Eur Respir J 1995; 8: 492-506.
2. Pellegrino R, Viegi G, Brusasco V, Crapo R, Burgos F et al. Interpretative strategies for lung function tests. Series ATS/ERS Task Force: Standardization of lung function
testing. Eur Respir J 2005; 26: 948-68.3. Cook CD, Hamann JF. Relation of lung volumes to height in healthy persons
between the ages of 5 and 38 years. J Pediatr 1961; 59: 710-14.4. Zapletal A, Samanek M, Paul T. Lung function in children and adolescents. Methods
and references values. Prog Respir Res 1987; 22: 83-112.5. Clausen JL. Prediction of normal values in pulmonary function testing. Clin Chest
Med 1989; 2: 135-43.6. Torres L, Martínez F, Manco J. Correlation between standing height, sitting height,
and arm span as an index of pulmonary function in 6-10-year-old children. PediatrPulmonol 2003; 36: 202-208.
7. Ip M, Karlberg E, Chan K, Karlberg J, Luk K et al. Lung function reference valuesin Chinese children and adolescents in Hong Kong. Am J Respir Crit Care Med2000; 162: 430-5.
8. Sylvester KP, Milligan P, Patey RA, Rafferty GF, Greenough A. Lung volumes inhealthy afro-caribbean children aged 4-17 years. Pediatr Pulmonol 2005; 40: 109-12.
9. DeGroodt E, Quanjer P, Wise M, van Zomeren B. Changing relationships betweenstature and lung volumes during puberty. Respir Physiol 1986; 65: 139-153.
10. Wang X, Dockery D, Wypij D, Gold D, Speizer F, et al. Pulmonary function growth velocity in children 6 to 18 years of age. Am Rev Respir Dis 1993; 148: 1502-8.
11. Degroodt E, van Pelt W, Borsboom G, Quanjer P, van Zomeren B. Growth oflung and thorax dimensions during the pubertal growth spurt. Eur Respir J 1988;1: 102-108.
12. Rosenthal M, Cramer D, Bain SH, Denison D, Bush A, Warner JO. Lung functionin white children aged 4 to 19 years: II. Single breath analysis and plethysmography.Thorax 1993; 48: 803-8.
13. Manzke H, Stadlober E, Schellauf HP. Combined plethysmographic and flow volumereference values for male and female children aged 6 to 16 years obtained from“hospital normals”. Eur J Pediatr 2001; 160: 300-6.
14. Jones R, Nzekwu M. The effects of body mass index on lung volumes. Chest 2006;130: 827-833.
15. Donnelly PM, Yang TS, Peat JK, Woolcock AJ. What factors explain racial differencesin lung volumes? Eur Respir J 1991; 4: 829-938.
16. Pool JB, Greenough A. Ethnic variation in respiratory function in young children.Respir Med 1989; 83: 123-25.
17. Yang TS, Peat J, Keena V, Donnelly P, Unger W, et al. A review of the rac ialdifferences in the lung function of normal Caucasian, Chinese and Indian subjects.
Eur Respir J 1991; 4: 872-880.18. Whittaker AL, Sutton AJ, Beardsmore CS. Are ethnic differences in lung functionexplained by chest size? Arch Dis Neonatal Ed 2005; 90: F423-28.
19. Eisner M, Forastiere F. Passive smoking, lung funct ion and public heal th. Letter. Am J Respir Crit Care Med 2006; 173: 1184-5.
20. Brutsaert TD, Soria R, Caceres E, Spielvogel H, Haas JD. Effect of developmentaland ancestral high altitude exposure on chest morphology and pulmonary functionin Andean and European/north American natives. Am J Hum Biol 1999; 11: 383-395.
21. Díaz A, Ceruti E, Duarte J. Ventilación pulmonar en niños normales. I. Volúmenespulmonares y distribución de la ventilación. Rev Chil Pediatr 1969; 40: 670-677.
22. Gutiérrez M, Rioseco F, Rojas A, Casanova D. Reference spirometric values for the Chilean popula tion at sea level. Rev Med Chile 1996; 124: 1295-1306.
23. Knudson R, Lebowitz M, Holberg C, Burros B. Changes in the normal maximalexpiratory flow-volume curve with growth and aging. Am Rev Respir Dis 1983;127: 725-734.
Determinación de valores de referencia para volumenes pulmonares en escolares y adolescentes159
nación de volúmenes pulmonares. El uso de valores predictivosinapropiados podría conducir a errores de comparación y
por lo tanto, en el tratamiento de estos pacientes, por lo queel empleo de las ecuaciones sugeridas por ATS y ERS para volúmenes pulmonares plantea un cuestionamiento sencillo:¿estaríamos también subestimando estos valores en niños
y adolescentes chilenos?. Creemos en la necesidad e impor- tancia de contar con ecuaciones de referencia propias para
determinar los volúmenes pulmonares en niños y adolescentes,y así establecer una correcta comparación y evaluación de la funcion pulmonar en pacientes con diversas condicionescrónicas y eventualmente agudas.

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 19/54
Resumen
La neumonía asociada a ventilación mecánica es una infección intrahospitalaria en pacientes deunidades críticas. Su presencia determina una mayor estadía hospitalaria, elevación de los costos deatención, mayor uso de antibióticos y un aumento en morbimortalidad. Las estrategias de prevenciónse encuentran en permanente revisión. La tasa de esta enfermedad ha mostrado una disminuciónsignificativa en nuestro medio durante los últimos 10 años. Existen diversos patógenos asociados asu etiología, siendo S. aureus y P. aeruginosa los mas frecuentes en Chile. Existen muchos factoresde riesgo identificados. Aunque no existe un criterio específico para su diagnóstico, se reconoce lapresencia de criterios clínicos y radiológicos. Todas las estrategias de prevención descritas handemostrado un efecto significativo. No existe una recomendación general para el tratamiento, porlo que esta debe basarse en la epidemiología local de cada unidad critica.
Palabras Claves: Neumonía, ventilación mecánica, niños.
disponible en http://www.neumologia-pediatrica.cl
NEUMOLOGIA PEDIATRICA ISSN 0718-3321
Neumonía asociada a ventilación mecánica en niñosDr. Luis Delpiano MéndezPediatra InfectólogoHospital San Borja Arriarán
Correspondencia: Dr. Luis Delpiano Méndez. Unidad de InfectologíaPediátrica, Hospital San Borja Arriarán. Email: [email protected]
160
DEFINICIÓN Y EPIDEMIOLOGÍA
La neumonía asociada a ventilación mecánica (NAVM), co-
rresponde a una infección intrahospitalaria en pacientes,
habitualmente de unidades críticas, que están o han recibido
apoyo ventilatorio invasivo por más de 24 horas y que no la
presentaban al momento de su intubación y conexión al
ventilador (1). Como infección nosocomial, determina una
mayor estadía hospitalaria en promedio (26,1± 17,3 vs.10,6 ± 6 días), elevación de los costos de atención médica,
mayor consumo de antimicrobianos y dado su gravedad,
determina un importante aumento en morbimortalidad(2).
Es una infección nosocomial denominada trazadora, y está
incorporada por el Ministerio de Salud (MINSAL) al sistema
de vigilancia activa de los hospitales nacionales, y su tasa o
indicador se expresa como el número de episodios de NAVM
por 1.000 días de ventilación mecánica (VM). Este valor, a
nivel de cada hospital del país, representa un referente de
evaluación relacionado a calidad de atención en el tiempo y
además permite su comparación con el indicador nacional o
estándar propuesto por el MINSAL; valor que correspondeal percentil 75 de años previos.
En la Figura 1, se aprecia la evolución de las tasas pediátricas
de NAVM en Chile revelando un descenso progresivo de
ellas desde 15 episodios en 1996 hasta 6 episodios por 1.000
días de VM el año 2006; valor aún ligeramente por sobre los
reportes extranjeros de países desarrollados pero inferior a
la obtenida en pacientes adultos que alcanzó en 2006 una
tasa de 22 episodios por 1.000 días de VM (3).
La NAVM representa habitualmente la segunda infecciónnosocomial de unidades de cuidados intensivos, por lo quesus estrategias de prevención se encuentran en permanentedifusión y supervisión. Hoy en día, se le menciona como unimportante indicador de calidad de atención al paciente fomentando la permanente mejoría de las prácticas relacionadasal cuidado del enfermo sometido a VM y el benchmarkingque permita modificar elementos que favorezcan la disminución
de brotes de NAVM y reducción de sus tasas (4).
ETIOLOGÍA
Algunos autores clasifican la NAVM en precoz o tardía si esque ésta aparece antes o después de 72 horas (hasta 5 díaspara otros) respectivamente, de intubación y soporte con VM. En los episodios precoces, se reconocen como etiologíaa diversos patógenos comunitarios de la vía respiratoria como:Streptococcus pneumoniae, Haemophilus influenzae y Moraxellacatarrhalis , agentes de la vía respiratoria alta probablementearrastrados al momento de la intubación, pero en general la
“verdadera” NAVM y en donde se focalizan las medidas deprevención estudiadas es en el fenómeno que aparece mas tardíamente. En este caso, las etiologías reconocidas sonStaphilococcus aureus y bacilos gram negativo como Pseudo-monas auruginosa, Klebsiella sp. y Enterobacter sp. entreotros(5).
En Chile durante el año 2006 y sobre una base de 99NAVM notificadas en servicios pediátricos y con identificaciónde etiología en el 90%, los agentes fueron S. aureus (21,3%),Pseudomonas aeruginosa (20,2%), A. baumannii (11,2%),Klebsiella pneumoniae (6,78%) entre otros. En neonatología;sin embargo, de 107 episodios notificados se identificó sólo
un 38,3% de etiologías, predominando A. baumannii (29,3%),

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 20/54
161
Figura 1.- Tasa de NAVM por 1.000 días de ventilación mecánica en serviciosde pediatría y neonatología. 1996 a 2006. MINSAL Chile.
16
12
8
4
0
t a s a p o r 1 0 0 0 d í a s V M
1 9 9 6
1 9 9 8
2 0 0 0
2 0 0 2
2 0 0 5
2 0 0 6
Pediatría Neonatología
Neumonía asociada a ventilación mecánica en niños
S. aureus (26,8%), y K. pneumoniae (12,2%)(3). No debe-
mos olvidar los virus respiratorios, frecuentes como etiología
a nivel nacional y en diferentes series publicadas.
FACTORES DE RIESGOLa mayoría de los estudios que identifican factores de riesgo
están basados en población adulta, muchos extrapolables a
niños y reconociendo entre ellos como mecanismos patogé-
nicos a la aspiración de secreciones orofaríngeas, aspiración
de flora gastrointestinal e inhalación de bacterias en aerosoles,
fenómenos facilitadores de la llegada de agentes patógenos
a la vía respiratoria inferior.
Particularmente los factores de riesgo dependientes de la
atención clínica son:
• Duración de la ventilación mecánica.
• Prolongada estadía en unidades críticas.
• Empleo de dispositivos venosos centrales.
• Exposición a antimicrobianos.
• Uso de bloqueadores H2..
• Re-intubaciones.
• Intubación naso-traqueal.
• Aspiración repetitiva de secreciones por traqueostomía.
• Traslados del paciente intubado fuera de la unidad.
En la población pediátrica, dos estudios identificaron como
factores de riesgo a la inmunodeficiencia, inmunosupresión
y al bloqueo neuromuscular (6) y también a la presencia de
síndromes genéticos asociados a bloqueo neuromuscular, re-
intubaciones, grandes quemados, y transporte fuera de la
unidad crítica(7). Sin embargo, el más importante factor de
riesgo es evidentemente la intubación traqueal ya que elimina
los mecanismos de defensa naturales y permite el ingreso de
potenciales bacterias patógenas
DIAGNÓSTICO
Claramente el establecer el diagnóstico de NAVM en niños
presenta mayor dificultad que en pacientes adultos. Así
entonces, para la definición de caso, debe existir un episodio
febril que apoye un cuadro infeccioso con sospecha de foco
pulmonar clínico y/o radiológico y el descarte de otra eventual
fuente de infección(1). El estándar de oro como es la biopsia
pulmonar resulta habitualmente impracticable y por tanto de
escasa ayuda clínica.
No existe un criterio específico, por tanto se consideran
varios elementos clínicos y radiográficos aplicables a niños,
explicitados en Tabla 1(1,8) . Aún así, la sensibilidad y especificidad
de ellos es pobre en comparación a la histopatología y no
valora por ejemplo huéspedes particulares como el niño
inmunocomprometido. Para mejorar el diagnóstico e identificar
etiología, estos criterios deben acompañarse de estudios
microbiológicos que en muestras obtenidas del árbol respi-
ratorio deben ser cuantitativos. Los criterios microbiológicos
en búsqueda de etiología incluyen:

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 21/54
162Delpiano L.
Tabla 1.- Criterios diagnósticos de NAVM en niños.
Edad Criterio
A) Menor de 1 año Cambio en el intercambio de oxígeno (aumento requerimiento, desaturación)
y al menos 3 de los siguientes:
1. inestabilidad térmica sin causa reconocible
2. leucopenia (< 4.000) o leucocitosis (> 15.000) y baciliformes ≥ 10%
3. aparición esputo purulento, o cambio de características o aumento en secreciones
4. apnea, taquipnea, aleteo nasal con retracciones
5. aparición sibilancias o roncus
6. tos
7. bradicardia o taquicardia (< de 100 ó > de 170 x`
más criterio radiológico:
Al menos 2 radiografías seriadas que muestren un nuevo o progresivo infiltrado pulmonar,
consolidación o cavitación o neumatocele *.
B) Mayor de 1 año Al menos uno de los siguientes criterios clínicos:
1. fiebre sin otra causa reconocible
2. leucopenia (< 4.000) o leucocitosis (> 12.000)
y al menos 2 de los siguientes:
1. aparición esputo purulento, o cambio en características o aumento en secreciones
2. tos, disnea, apnea o taquipnea
3. estertores o roncus
4. cambio en el intercambio gaseoso: desaturación, mayor requerimiento oxígeno
más criterio radiológico:
Al menos 2 radiografías seriadas que muestren un nuevo o progresivo infiltrado pulmonar,
consolidación o cavitación o neumatocele*.
* En niños no afectados por patología cardiaca o pulmonar previa se requiere sólo una radiografía de tórax.
a) Hemocultivo positivo sin otra causalidad.
b) Cultivo positivo de líquido pleural.
c) Cultivo positivo de lavado broncoalveolar (LBA).
d) Mas de 5% de células con bacterias intracelularesobtenidas por LBA.
e) Estudio histopatológico (neumonía, absceso) o cultivo
bacteriano positivo o visualización de hifas.Respecto de los estudios microbiológicos cuantitativos, mas
difíciles de obtener que en pacientes adultos, el aspiradoendotraqueal a través de traqueostomía tiene alto riesgo decontaminación por patógenos de la vía respiratoria alta(1). Losotros métodos endoscópicos tienen mayor soporte enpacientes adultos y los valores o puntos de corte se exponenen la Tabla 2(9). El único reporte prospectivo en poblaciónpediátrica(10) que evaluó estudio endoscópico con cepilloprotegido o LBA en 103 niños con criterio clínico de NAVM,reveló interesantes hallazgos como que la inespecífica presenciade secreciones traqueales purulentas estuvo presente en el50% de los pacientes sin neumonía bacteriana; en segundo
lugar que los aspirados fueron sensibles pero no específicospara neumonía bacteriana (sensibilidad 93% y especificidad41%) y tercero, que con puntos de corte de 103 UFC/mlpara cepillo protegido y 104 UFC/ml para LBA con más de1% de células con bacterias intracelulares se obtiene unasensibilidad de 90% y especificidad de 88%. Este ensayo tiene como limitación, el incluir pacientes de un sólo centroy ejecutado por un único endoscopista respiratorio. Por lo
anterior, cada centro debe contar con criterios definidosdesde el punto de vista clínico, radiológico y microbiológicode acuerdo a su disponibilidad y además diferenciar episodiosde colonización de aquellos de infección verdadera.
MEDIDAS DE PREVENCIÓN
Las consecuencias clínicas, económicas y legales justificansobremanera la incorporación y mantención de estrategiasde prevención de NAVM. Como en la mayoría de las infec-ciones hospitalarias, las medidas básicas cobran gran importanciaen su control. El lavado de manos antes y después de manipularal paciente o su unidad con jabones antisépticos o alcohol

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 22/54
163
Tabla 2.- Cultivos cuantitativos de secreciones respiratorias bajas en pacientes adultos con diagnóstico de NAVM.
Técnica diagnóstica Sensibilidad Especificidad VPP VPN
Cultivo cepillo protegido (≥ 103 UFC /ml) 82% 89% 90% 89%
Cultivo LBA (≥ 104 UFC/ml) 91% 78% 83% 87%
Microscopía en LBA ≥ 5% microorganismos intracelulares 91% 89% 91% 89%
Neumonía asociada a ventilación mecánica en niños
VPP: Valor predictivo positivo; VPN: Valor predictivo negativo.
gel, el empleo de guantes y eventualmente mascarilla almomento de manipular la traqueotomía constituyen medidasprimarias(1,11).
Recientemente en adultos, se han establecido “bundles”que incorporan sólo 4 medidas con gran impacto en preven-ción de NAVM y que son: Mantener elevación de la cabeza
30 a 45º, reducir sedación y/o bloqueo neuromuscular transitoriamente durante el día y tener protocolos de extu-bación, mantener profilaxis para úlceras de stress y mantenerprofilaxis de trombosis venosa profunda. Sin embargo, existecarencia de reportes relacionados a bundles en niños.
Claramente entre las estrategias generales de prevención,cuyo objetivo es evitar la contaminación del paciente y evitarla emergencia de patógenos resistentes en los hospitales tenemos:
a) Prevenir la difusión iatrogénica: Instaurando higiene demanos como medida supervisada, práctica que ha demostradoestadísticamente la disminución de infección nosocomial(12),pero que desafortunadamente no se cumple al 100%. Res-pecto del insumo para el lavado de manos, la instalación dedispensadores de alcohol gel facilitan la adherencia y se le hademostrado ser superior al agua y jabón. El uso de guantescomo barrera aunque efectivo, por sí sólo tiene menorimpacto que el lavado de manos por lo que debieran em-plearse en forma sinérgica como medida de prevención(13).
b) Reducción de emergencia de microorganismos resis- tentes: Evitar el uso indiscriminado de dispositivos invasivoscomo catéteres venosos centrales, líneas arteriales y catéteresurinarios entre otros, ya que facilitan la colonización bacterianapor lo que debieran ser retirados lo antes posible. Así también,
los profesionales involucrados deben mantener la técnicaaséptica y las barreras necesarias durante la instalación deestos dispositivos. Otro pilar importante, lo constituye laestrategia de trabajo con una política de uso racional deantimicrobianos evitando presión selectiva y desarrollo deresistencia microbiana(14).
Estrategias puntuales dirigidas a prevención de NAVMincluyen:
a) Posicionamiento semisentado del paciente: El supino facilita neumonía por mayor riesgo de reflujo gástrico. Estamedida ha sido corroborada en pacientes adultos mejorando
además la optimización del volumen corriente y la apariciónde atelectasias. No existen datos específicos en poblaciónpediátrica, se debe tener cuidado en pacientes sometidos acirugía cardiotorácica por las consecuencias hemodinámicas,pero para la mayoría de los pacientes en unidades críticasesta intervención parece ser beneficiosa y de bajo riesgo,
recomendándose 15 a 30º en neonatos y 30 a 45º en niños.b) Drenaje de secesiones subglóticas, bajo el postulado
de que las secreciones acumuladas en esta zona y alrededordel tubo traqueal se pueden colonizar y posteriormente seraspiradas ocasionando neumonía, su remoción permanentereduciría la incidencia de esta complicación. Esta prácticarequiere de tubos especialmente diseñados que incorporanun lumen que permite la aspiración continua. Un recientemeta análisis, evaluó esta conducta en 5 estudios que incluyerona pacientes adultos demostrando reducción significativa en tasas de NAVM(15). Aún esta pendiente su validación en lapoblación pediátrica.
c) Profilaxis de úlceras de stress. De amplia evaluación enadultos con ensayos y meta análisis comparando bloqueadores
H2 y sucralfato muestran una amplia variedad de resultadose impacto en reducción de NAVM y letalidad asociada,promoviendo su indicación a pacientes con factores de riesgoparticulares como aquellos con shock, coagulopatías y fallarespiratoria(14) . Sólo un reporte retrospectivo no mostróefecto de la profilaxis para úlcera de stress en la incidenciade NAVM en niños que recibieron ranitidina, sucralfato oplacebo(16).
d) Otras dos estrategias, con algún impacto en adultosson la higiene de la cavidad oral con clorhexidina y la descon-
taminación digest iva select iva. Si bien es cierto la primeramedida ha mostrado en disminuir la neumonía del postradoy la NAVM en pacientes cardioquirúrgicos, requiere deestudios bien diseñados en niños y no debiera emplearse enneonatos. La descontaminación selectiva con diversas moda-lidades como antibióticos tópicos asociados o no a parenterales,resultados expuestos en gran número de experiencias y otros
tantos metaanálisis muestran impacto en reducción de tasase incluso mortalidad(17), datos que nuevamente no estándisponibles en niños y que originan detractores ante la eventualemergencia de resistencia futura.
e) Medidas destinadas al manejo de los circuitos del ventilador mecánico incluyen: cambio de circuito semanal o

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 23/54

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 24/54
Resumen
La reemergencia de la tuberculosis a nivel mundial se vincula a diferentes factores dentro de loscuales está la infección VIH, esto también se ve reflejado en la población pediátrica, planteandodificultades en el diagnóstico y tratamiento oportuno, lo que obliga a tratar a nuestros niños por unequipo multidisciplinario.
Palabras Claves: Tuberculosis, SIDA, manifestaciones, niños.
disponible en http://www.neumologia-pediatrica.cl165
NEUMOLOGIA PEDIATRICA ISSN 0718-3321
Tuberculosis y SIDA en el niñoDra. Julia Villarroel BarreraPediatra InfectólogaHospital Clínico Félix Bulnes
Correspondencia: Dra. Julia Villarroel Barrera. Pediatra Infectóloga. HospitalClínico Félix Bulnes. Email: [email protected]
INTRODUCCIÓN
La tuberculosis (TBC) es una enfermedad que se creíacontrolada, pero en las últimas décadas ha sufrido un incre-mento considerable debido a varios factores, tales como lapobreza, la limitada atención en salud, las constantes migra-ciones, el hacinamiento y en el último tiempo se ha agregadola pandemia de SIDA (1).
Los infectados con el virus de inmunodeficiencia humano(VIH), tienen 5 a 7 veces mayor posibilidad de adquirir laTBC que la población general, donde la frecuencia es de 3a 5% versus 17 a 37% cuando coexisten ambas infecciones.La tuberculosis puede aparecer en cualquier etapa de lainfección VIH y tampoco no constituye una enfermedadindicadora de SIDA.
EPIDEMIOLOGÍA
La TBC continúa siendo un problema de salud pública, se haproducido una reemergencia de esta patología, especialmentedespués de la epidemia de SIDA. La OMS debió postergarla meta que tenía de erradicar la TBC en el año 2000 y hadeclarado este problema como una emergencia global(2). Seestima que un tercio de la población mundial porta el bacilode Koch en forma latente, se originan más de 8 millones decasos nuevos por año, de los cuales 800.000 son niños.
Durante el año 2002 hubo 600.000 niños muertos por SIDAen el mundo, 200.000 estaban co-infectados con TBC (3).
Si el riesgo de desarrollar TBC en una persona infectadacon M. tuberculosis es de 10% en toda la vida, al estar co-infectado con VIH este riesgo asciende a 10% por año. Secalcula que en el mundo habrá un exceso de 80 a 100millones de casos nuevos sólo por la asociación de TBC ySIDA y se producirán más de 30 millones de muertes(3). Lossujetos infectados con VIH tienen 5 a 7 veces mayor frecuencia
de adquirir una TBC. En la población general tras la exposiciónal Mycobacterium tuberculosis el 3-5% desarrollaran la enfer-medad activa, en cambio en los pacientes VIH positivos el17-37% tendrán TBC en los cuatro meses siguientes a laexposición.
En el continente americano se aprecia una situación variable,algunos países presentan tasas superiores a 85 x 100.000como Bolivia, Ecuador, Haití, República Dominicana y Hon-duras y otros con tasas menores a 24 x 100.000 como CostaRica, Cuba, Chile, Uruguay, EE.UU, Canadá, Jamaica y PuertoRico.
En nuestro país se ha producido un descenso sostenido
en la morbilidad y mortalidad en todas las edades, con tasasde 18,4 x 100000, cifras que lo sitúan como un país de bajaendemia(2). La co-infección VIH y TBC es de 3% a los 15años y de 6% a los 30 años, la disminución de la incidenciade TBC y el aumento moderado de la infección VIH registradoen Chile en los últimos años a condicionado una tasa de co-infección relativamente baja.
FISIOPATOLOGÍA
La mayor susceptibilidad de los pacientes infectados con VIHpara contraer TBC se ha relacionado con una disminuciónen los linfocitos T1 lo que ocasiona un descenso en la
producción de interferón gama, el interferón gama es funda-mental en las defensas contra los mycobacterium.
Por otra parte, los macrófagos representan la primera líneade defensa contra la TBC, son responsables de la fagocitosisdel bacilo, inhiben el crecimiento, procesan y presentan elantígeno a las células efectoras, activan los CD4 y liberancitokinas como interleukina 2 (IL-2) e interferón gama.
En los pacientes VIH positivos hay una profunda alteración funcional del sistema macrofágico de tal manera que no escapaz de ejercer las funciones antes mencionadas y el M.
tuberculosis induce al macrófago a producir factor de necrosis
tumoral, IL-1, IL-6, sustancias pro-inflamatorias que van a

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 25/54
166
Figura 1.- Fisiopatologia de TBC
Linfocitos T1 Macrófago Linfocito T2
1nterferón gama Fagocita bacilo, presentan 1L-4, 1L-10antígenos, inhibe crecimiento,
activan CD4, liberan 1L-2,
1nterferón gama
Control de la infección tuberculosa
Figura 2.- Fisiopatologia de la TBC y SIDA
Alteración funcional Estimulación macrófago
Interferón gama Aumento IL-1, IL-6, FNT
Protección> replicación viral
bacilo de Koch
Tuberculosis y SIDA en el niño
FNT: Factor de necrosis tumoral.
oc asionar una mayor replicación del virus VIH en las zonas
infectadas por el bacilo tuberculoso(4,5) (Figuras 1 y 2).
MANIFESTACIONES CLÍNICAS
En los niños es siempre difícil el diagnóstico de tuberculosis,
esto se ve agravado más aún cuando coexisten la TBC y la
infección por VIH, ya que, la sintomatología se hace atípica
en la medida que disminuye la inmunidad, apareciendo formas
miliares y localizaciones extrapulmonares (36%), como son
el compromiso del sistema nervioso central (SNC) (15%) o
la TBC de piel y osteoarticular, dos formas que han resurgido
en los últimos años en asociación con la pandemia de SIDA (6-
9). Es importante considerar que el 40% de los niños VIH
positivo presentan patología pulmonar con imágenes radio-lógicas persistentes, lo que hace aún más difícil el diagnóstico.
En la edad pediátrica deberíamos sospechar la tuberculosis
en un niño infectado con el virus VIH cuando presenta fiebre
persistente por más de una semana (75%), taquipnea, ade-
nopatías periféricas, pérdida de peso superior al 10%, man-
tenida por más de tres meses y la persistencia de imágenes
pulmonares a pesar de tratamientos bien llevados. También
se debe descartar una infección por el bacilo tuberculoso
cuando hay adultos en la casa que son tosedores crónicos(10).
La tuberculosis pulmonar en estados precoces puede mostrar
un patrón clínico y radiológico que no difiere de los pacientes
no infectados por VIH. Se puede presentar como una neu-monía no resuelta, infiltrados pulmonares difusos, linfoadeno-
patías torácicas que pueden ser relevantes en los VIH positi-
vos(10-11).
La forma abdominal, produce lesiones viscerales, linfoade-
nopatías y necrosis visceral, lo que se visualiza mejor con un
TAC. En contraste, la ascitis es característica de la TBC
abdominal en los pacientes VIH negativos(11). En cuanto a las
manifestaciones clínicas de meningitis tuberculosa, estas son
semejantes en los VIH positivos así como en los negativos,
excepto por las lesiones de masas intracerebrales las que son
más frecuentes en los pacientes co-infectados. El compromiso
meníngeo es 5 veces más frecuente en los co-infectados enáreas endémicas. La meningitis se puede desarrollar incluso
en pacientes que están recibiendo terapia antituberculosa,
esto se explica por la presencia de tuberculomas que se
rompen en el espacio subaracnoídeo, o por la interacción
de drogas que impiden concentraciones adecuadas de los
medicamentos antituberculosos en el líquido cefalorraquideo.
Las alteraciones en el LCR son semejantes en pacientes VIH
positivos y negativos. Los niños co-infectados presentan
sintomatología meníngea a edades menores, la sintomatología
es de evolución más corta y en general tienen PPD negativo.
El pronóstico es muy malo, con 30% de mortalidad y los
sobrevivientes presentan graves secuelas(10,11).
En zonas endémicas la TBC extrapulmonar se manifiesta
más frecuentemente por linfoadenopatías, compromiso óseo,
meníngeo, pericárdico, peritoneo y pleura(11). En hijos de
madres VIH positivas con tuberculosis activa, se puede
presentar en el recién nacido un cuadro de tuberculosis
congénita, esta forma puede resultar por la diseminación
hematógena secundaria a micobacteriemia materna, rotura
de un tubérculo placentario en la circulación fetal o por la
deglución in útero de líquido amniótico. La madre puede no
tener sintomatología y estar cursando una forma subclínica
genital, resultando en un recién nacido con síntomas inespe-
cíficos, como inapetencia, falla en el crecimiento, fiebre,

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 26/54
167 Vi ll ar ro el J.
Figura 3.- Neumonía condensante del segmentoapical del lóbulo inferior izquierdo asociada aTBC.
Figura 4.- Milia pulmonar y condensación enlíngula asociada a TBC.
hepatoesplenomegalia, neumonía, meningitis y en ocasiones
puede debutar como un distres respiratorio, apneas, ictericia
y distensión abdominal(12).
EXÁMENES DE LABORATORIO
El diagnóstico de TBC es siempre difícil en los niños, más
aún si co-existen con la infección por VIH.
• Las baciloscopías en general tienen baja sensibilidad (30
60%) y especificidad (50%), ya que, a esta edad la
infección es poco bacilífera y este examen requiere para
visualizar el bacilo de Koch entre 5000 a 10000 baci-
los/ml. de muestra, por lo tanto una baciloscopía negativa
no descarta el diagnóstico. No permite diferenciar entre
M tuberculosis y otros bacilos atípicos. La baciloscopía
de contenido gástrico es positiva en menos del 20%
de los casos. Las baciloscopías en muestras extrapul-
nares como nódulos linfáticos, LCR, líquido articular
son positivas en menos del 25%(13).
• Lavado bronco-alveolar presenta una positividad de 80-
90%.
• L os cultivos pueden ser con medios convencionales,
como el de Loewenstein-Jenssen, método que requiere
de una observación no menor de ocho semanas, o en
medios líquidos radiométricos que acortan el tiempo a
10 días. Cuando el número de bacilos es considerable
y permite tener baciloscopías positivas, ambos métodos
tienen igual rendimiento, pero si las baciloscopías son
negativas o frente a infecciones por mycobacterias
atípicas los medios de cultivo líquidos son los mejores(13).
• Reacción en cadena de polimerasa (RPC) es costosa,
no reemplaza a los métodos tradicionales y está aprobada
por la FDA para uso solo en muestras respiratorias o
en pacientes que han recibido menos de siete días de
tratamiento antituberculoso. Su sensibilidad y especificidad
es de 95% cuando las baciloscopías son positivas, pero
si las baciloscopías son negativas la sensibilidad bajaalrededor del 50%(14-17).
• Radiografía de tórax se observa alterada en el 90% de
los casos de TBC pulmonar , con infiltrados insterticiales
difusos o localizados muy semejantes a los descritos en
la neumocistosis, se aprecian además linfoadenopatías
torácicas, compromiso de varios lóbulos (25%) y com-
promiso pleural (20%); sin embargo en pacientes con
SIDA avanzado y TBC la radiografía de tórax es nor-
mal(17,18) (figura 3 y 4).
• Ecografía abdominal, demuestra las adenopatías y laslesiones necróticas viscerales.
• Scanner abdominal, permite localizar mejor las lesiones
necróticas intraabdominales.
• Scanner cerebral, en los casos de meningitis tuberculosa
muestra el compromiso ventricular y la gran atrofia glial
y cerebral.
• Biopsias ganglionares.
• PPD: en los pacientes VIH positivo sólo el 10 a 35%
son PPD positivo. El PPD no ayuda en el diagnóstico,

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 27/54
168Tuberculosis y SIDA en el niño
pero una induración mayor o igual a 5 mm. es conside-
rada positiva. Un PPD negativo en un paciente VIH
positivo no descarta la infección ya que el 50% de las
TBC miliares y meníngeas tienen PPD negativo y lo
mismo se aprecia en los niños menores de 2 años(17).
• Hemocultivos con técnica especial para el aislamiento
del mycobacterium, es de utilidad en las formas disem
nadas y febriles.
TRATAMIENTO
Tratamiento profiláctico
L a profilaxis se describe efectiva para reducir la morbimortalidad
por TBC en los pacientes con infección por VIH, pero el
efecto protector desaparece rápidamente una vez que es
suspendida. En los pacientes VIH positivo con PPD negativo
la profilaxis no reduce el riesgo de infección tuberculosa. La
quimioprofilaxis se recomienda en recién nacidos hijos de
madres bacilíferas positivas, pacientes VIH positivos con PPD
positivo mayor de 5 mm y en pacientes VIH positivos con
PPD negativo pero con antecedentes de contacto tuberculoso.
Se debe administrar Isoniazida (5 mgr/kg/día) por 9 a 12
meses o Rifampicina (10 mgs/kg/día) asociado a Pirazinamida
(15 mgs/kg/día) administrado 2 veces por semana durante 2
meses, ambos esquemas serían igualmente efectivos, aunque
este último produciría mayor compromiso hepático. Antes
de efectuar quimioprofilaxis se debe descartar siempre una
TBC activa, efectuar exámenes tendientes a medir la función
hepática y conocer la interacción con otros medicamentos(20).
Tratamiento de la enfermedad tuberculosa
En los pacientes inmunocompetentes, la participación activa
del sistema inmunitario celular del huésped juega un rol
fundamental en el proceso de curación. En el paciente
inmunocomprometido es importante considerar que la terapia
debe ser iniciada precozmente y no solo en los casos en que
se produjo aislamiento del Mycobacterium, sino también
cuando hay fundadas sospechas clínicas. Se deben utilizar
antimicrobianos bactericidas, la terapia debe ser asociada para
evitar la resistencia y controlada para asegurar que efectiva-
mente se cumpla(21,22).
En pacientes infectados con VIH y TBC ocasionada por
bacilos susceptibles se recomienda una duración del trata-
miento de por lo menos 9 meses, si por el contrario, la clínica
y la respuesta bacteriológica no son buenas, el tratamiento
debe prolongarse más de 12 meses o mantenerse hasta
cuatro meses después que los cultivos se hacen negativos(21,22).
En las formas pulmonares graves o de localización extrapul-
monar se deben administrar 4 drogas por 2 meses y luego
2 fármacos por 10 meses, incluso hasta dos años si los bacilos
son resistentes.
En las formas meníngeas y del SNC el tratamiento es con
4 drogas donde se incluye la Estreptomicina por un periodo
de 2 meses, con una duración total del tratamiento de 10 a
12 meses(21,22) . Generalmente se esteriliza la expectoración
entre uno y tres meses y se producen fracasos de tratamiento
en el 15% de los casos.
Se debe iniciar primero el tratamiento antituberculoso y
posponer el tratamiento antiretroviral a lo menos 4 a 8
semanas. En los casos en que el paciente está con terapia
antiretroviral esta se puede suspender para iniciar el tratamiento
antituberculoso, si esto no es posible, se deben adecuar las
drogas antituberculosas para que no se produzcan interaccio-
nes, por lo que siempre es aconsejable en los casos de co-
infección que el tratamiento se evalúe en conjunto con
médicos infectólogos y broncopulmonares(21,22).
Es importante recordar que las drogas de primera línea en
el tratamiento antituberculoso actúan en diferentes niveles
de la multiplicación del bacilo de Koch. La Isoniazida esbactericida, actúa en la fase de rápida multiplicación de los
bacilos y alcanza elevadas concentraciones en LCR semejantes
a las concentraciones en el suero. Rifampicina también actúa
en la fase de multiplicación rápida, alcanza concentraciones
en el LCR 20% de las del suero pero estas son suficientes.
La Pirazinamida actúa sobre los bacilos que están en lenta
multiplicación y los que están contenidos en los macrófagos
y en el ambiente ácido del casium, alcanza concentraciones
adecuadas en el LCR. El Etambutol ayuda a prevenir la
resistencia a la Rifampicina, penetra al LCR sólo con meninges
inflamadas(21-23).
Hay que considerar las interacciones medicamentosas, es
así como la Rifampicina induce actividad del citocromo P450
lo que disminuye la concentración de los inhibidores de
proteasas y de los inhibidores de transcriptasa reversa no
nucleósidos, por lo que no es recomendable usarlos juntos.
El uso de Rifampicina y Nevirapina juntas debe ser sólo
cuando no hay otras opciones terapéuticas(11,17,19,21,22) .
Los efectos adversos de la terapia antituberculosa son
menos frecuentes en los niños que en los adultos, se ven
especialmente con la asociación de Rifampicina e Isoniazida.
Se pueden producir los siguientes efectos:
• Compromiso hepático, evidenciado por la elevación
de las transaminasas o por la aparición de ictericia. Se
deben suspender temporalmente los medicamentos,
se ve más frecuentemente con Isoniazida (10 a 20%)
y aparece entre 60 a 90 post tratamiento, en cambio
para Rifampicina la incidencia es de 1-4% y aparece
entre 8-10 días postratamiento.
• Alergias, se pueden producir con la Estreptomicina y
en menor grado con la Isoniazida y Pirazinamida. La
Rifampicina ocasiona alergias cuando se administra en

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 28/54
169 Vi ll ar ro el J.
dosis altas, los exantemas que se presentan con estas
drogas son generalmente máculo-papulares.
• Toxicidad auditiva ocasionada por la Estreptomicina,
compromete el sistema vestibular, produce mareos y
vértigos y es reversible. Cuando se prolonga la toxicidad
se compromete el nervio coclear y esta es irreversible.
• Toxicidad renal, dada por el uso de Estreptomicina,
se produce un daño tubular.
• Parestesias bucales, ocasionadas por el uso de Estrep-
tomicina.
• Reacciones inmunológicas severas como trombocitop
nia, anemia hemolítica, insuficiencia renal aguda.
• Poliartralgias, son ocasionadas por la Pirazinamida en
40% de los casos, se ven en la primera fase del trata-
miento.
• Neurotoxicidad periférica, es raro con frecuencias de
0,2%, es más común cuando hay patología neurológica
agregada, se recomienda usar Piridoxina.
• Neuritis retrobulbar es ocasionada por el Etambutol,
hay una disminución en la agudeza visual o alteraciones
en la visualización de los colores verde y rojo.
• Hiperuricemia ocasionada por la Pirazinamida(22-24).
• Síndrome de reconstitución inmune, se produce durante
el tratamiento antituberculoso, se aprecia un deterioroclínico, con reaparición de la sintomatología previa,
aumento del PPD, aumento de los infiltrados pulmo-
nares, adenopatías periféricas y mediastínicas. Se ve en
el 36% de los pacientes que están recibiendo terapia
antituberculosa y terapia anti VIH versus sólo el 7% de
los pacientes que reciben sólo terapia antituberculosa.
Esta reacción es autolimitada pasa en 10 a 40 días, en
los casos en que la reacción es severa se debe indicar
corticoides(25-27).
Se han usado quinolonas tales como Ciprofloxacino en el
tratamiento antituberculoso, han sido bien tolerados y no sehan asociado a artropatías(28,29). Tendrían indicación en los
casos de resistencia o intolerancia a drogas de primera línea.
Una alternativa al uso de la Rifampicina en el tratamiento
de todas las formas de TBC, es el Rifabutin, su uso en pediatría
es limitado, también aumenta el metabolismo hepático de
muchas drogas pero es un inductor menos potente del
citocromo P450 que la Rifampicina. La co- administración de
Rifabutin con ciertas drogas como los inhibidores de proteasas
puede resultar en aumento de los niveles de Rifabutin, por
lo que se debe disminuir la dosis en 50%. No debe ser usado
junto a Fluconazol.
Dentro de las drogas de segunda línea que se han probado
en pediatría está la Cicloserina que tendría indicación cuando
hay compromiso hepático, alcanza concentraciones en el
LCR semejantes al suero, puede desencadenar psicosis y
crisis convulsivas.
El uso de corticoides en TBC está indicado en meningitis, tuberculosis abdominal, pericarditis, TBC diseminada y en
TBC endobronquial o con atelectasias. Se indica prednisona
(2 mgr/kg/d) durante 2 semanas y luego se reduce a un cuarto
de la dosis semanalmente hasta suspender.
SEGUIMIENTO
Es importante efectuar un control clínico y bacteriológico
mensual para ver la respuesta a la terapia. Se deben medir
las pruebas hepáticas mensualmente, si se produjera elevación
de las transaminasas en niveles menores a 3 veces el nivel
basal no se requiere suspender las drogas, con nivelessuperiores a 4 veces el nivel basal de las enzimas hepáticas
se deberían discontinuar las drogas antituberculosas. La
radiografía de tórax debe ser controlada según el caso lo
amerite, es importante considerar que una radiografía de
tórax normal no es criterio para discontinuar la terapia y que
las adenopatías hiliares pueden persistir por 2 a 3 años.
CONCLUSIONES
Podemos concluir que los pacientes pediátricos infectados
por VIH y TBC son complejos, requieren de un equipomultidisciplinario para decidir su tratamiento, que el tratamiento
debe ser vigilado para evitar recaídas y resistencia. Pero por
otro lado es necesario lograr avances en la investigación que
nos permitan disponer de técnicas de diagnóstico rápido, uso
de inmunomoduladores que permitan efectuar tratamientos
acortados y poder disponer de nuevas vacunas que nos
permitan lograr las metas propuestas por la OMS para el siglo
21.
REFERENCIAS
1. De Cock K, Binkin N, Zuber P, Tappero J, Castro K. Research Issues Involving HIV- Associated Tuberculosis in Resource- Poor Countries. JAMA 1996; 276: 1502-1507.
2. Programa nacional de control de la Tuberculosis 2005. Manual de organización ynormas técnicas. Ministerio de salud. Gobierno de Chile.
3. Donald P. Childhood tuberculosis: out of control? Current Opinion PulmonaryMedicine 2002; 8: 178-182.
4. Kaufmann S. Protection against tuberculosis: cytokines, T cells, and macrophages. Anna ls of the Rheu mati c Disease s 2002 ; 61 (sup plement 11): ii5 4-ii 58.
5. Jo E, Park J, Dockrell H. Dynamics of cytokine generation in patients with activepulmonary tuberculosis. Current Opinion Infectious Diseases 2003; 16: 205-210.
6. Mukadi Y, Wiktor S, Coulibaly I, Coulibaly D, Mbengue A, Folquet A, et al. Impactof HIV infection on the development, clinical presentation, and outcome of tuberculosis among children in Abidjan, Cote d'Ivoire. Aids 1997; 11: 1151-58.
7. Espinal M, Reingold A, Perez G, Camilo E, Soto S, Cruz E, et al. Humanimmunodeficiency virus infection in children with tuberculosis in Sant Domingo,Dominican Republic: prevalence, clinical findings and response to antituberculosis treatment. J Acquire Immune Defic Syndr Hum Retrovir al 1996; 13: 155-9.

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 29/54
170Tuberculosis y SIDA en el niño
8. Barbagallo J, Tager P, Ingleton R, Hirsch R, Weinberg J. Cutaneous Tuberculosis:Diagnosis and Treatment. Am J Clin Dermatology 2002; 3: 319-328.
9. Jellis J E. Human Immunodeficiency Virus and Osteoarticular Tuberculosis. ClinOrthopedics & Related Research 2002; 1: 27-31.
10. Chan S, Birnbaum J, Rao M, Steiner P. Clinical manifestati on and outcome of tuberculosis in children with acquired immunodeficiency syndrome. Pediatr InfectDis J 1996; 15: 443-447.
11. Garay J. Clinical presentation of pulmonary tuberculosis in under 10s and differencesin Aids-related cases: a cohort study of 115 patients. Trop Doct 1997; 27: 139-
142.12. Adhikan M, Pillay T, Pillay DG. Tuberculosis in the newborn: an emerging problem.Pediatr Infect Dis 1997; 16: 1108-12
13. Thomson R. Laboratory diagnosis of respiratory infections. Current OpinionInfectious Diseases 1999; 12: 115-119.
14. Wang S, Tay L. Early identification of Mycobacterium tuberculosis complex inBACTEC cultures by ligase chain reaction. Journal of Medical Microbiology 2002;51: 710-712.
15. Venkataraman P, Herbert D, Paramasivan C. Evaluat ion of the Bactec rad iome- tric method in the early diagnosis of Tuberculosis. Ind ian J Med Res 1998; 108 :120-7.
16. Kampmann B, Douglas Y. Chilhood tuberculosis: advances in immunopathogenesis, treatment and prevention. Current Opinion in Infectious Diseases 1998; 11: 331-335.
17. Havlir D, Barnes P Current Concepts: Tuberculosis in Patients with HumanImmunodeficiency Virus Infection. N Engl J Med 1999; 340: 367-373.
18. Ferrer J. Tuberculous Pleural Effusion and Tuberculous Empiema. Seminars inRespiratory and Critical Care Medicine 2001; 22: 637-646.
19. Chan S, Birnbaum J, Rao M, Stenner P. Clinical mani festation and outcome of
Tuberculosis in Children with acquired immunodeficiency syndrome. Pediatr InfectDis J May 1996; 15: 443-7.
20. Kaplan J, Masur H, Holmes K. Guidelines for the Prevention of OpportunisticIn fect ions Among HIV- In fected Persons-2002. USPHS / IDSA.
21. Mofenson L, Oleske J, Serchuck L, Van Dyke R, Wilfert C. Treating OpportunisticInfections Among HIV-Exposed. MMWR 2004; 53(RR 14): 1-63.
22. Treatment of Tuberculosis. American Thoracic Society, CDC, and Infectious DiseasesSociety. MMWR 2003; 52 (RR11): 1-77.
23. Squire S, Davies P. Treatment for mycobacterial infect ions. Current Opinion inInfectious Diseases 1998; 11: 159-162.
24. Van Scoy R, Wilkowske C. Antimycobacterial Therapy. Mayo Clinic Proceedings1999; 74: 1038-1048.
25. Furrer H, Malinverni R. Systemic Inflammatory Reaction after Starting Highly Active Antiretroviral Therapy in Aids Patients Treated for Extrapulmonary Tuberculosis. Am J Med 1999; 106: 371-372.
26. Hirch H, Kaufmanm G, Sendi P, Battegay M. Immune Reconstitution in HIV InfectedPatients. Clin Infect Dis 2004; 38: 1159-66
27. Kindelán J. Síndrome de reconstitución inmunológica. Enf Emerg 2003;5:214-21628. Chalumean M, Tomreleir S, d' Athis P, et al. Fluoroqu inolone safe ty in pediatr
patients: a prospective, multicenter comparative cohort study in France. Pediatrics2003; 111: 714
29. Congeni BL, Thomson RB. Fluoroquinolone: considerations for future use. PediatrInfect Dis J. 2002; 21: 345-6

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 30/54
Optimiza el aporte del fármaco a los pulmones
minimizando los costos, los efectos secundarios,
las dificultades de coordinación y los problemas
de portabilidad, mejorando la eficacia del
tratamiento.Mascarilla desilicona flexible
Adaptador universal al MDI
Válvula espiratoriaunidireccional
Válvula inspiratoriaunidireccional de bajaresistencia
CÁMARA DE RETENCIÓNCON VÁLVULA
abcd

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 31/54
Dra. Vivian Luchsinger PhDPrograma de VirologíaInstituto de Ciencias BiomédicasFacultad de MedicinaUniversidad de Chile.
NEUMOLOGIA PEDIATRICA ISSN 0718-3321
Conociendo al VRS
disponible en http://www.neumologia-pediatrica.cl 171
REFERENCIAS
1. Collins P, McIntosh K and Chanock R. Respiratory syncytial Virus. En: Fields Virologyde Fields BN, Knipe D, Howley P et als. Ed. Lippincott- Raven Publishers, Philadelphia,
EE.UU. 3ª'bb ed. 1996; 1313-1345.2. Sullender W. Respiratory syncytial Virus genetic and antigenic diversity. Clin Microbiol
Rev 2000; 13: 1-15.3. Cane P and Pringle C. Molecular epidemiology of respiratory syncytial virus: rapid
identification of subgroup A lineages. J Virol Methods 1992; 40: 297- 306.4. Peret T, Hall CB, Schnabel K, Golub J and Anderson L. Circulation patterns of
genetically distinct group A and B strains of human respiratory syncytial virus in acommunity. J Gen Virol 1998; 79: 2221-29.
5. Venter M, Madhi S, Tiemessen C and Schoub B. Genetic diversity and molecularepidemiology of respiratory syncytial virus over four consecutive seasons in South Africa: identifi cation of new subgroup A and B genotypes. J Gen Virol 2001; 82:2117- 24.
6. Zlateva K, Lemey P, Vandamme A and Van Ranst M. Molecular evolut ion andcirculation patterns of human respiratory syncytial virus subgroup A: positivelyselected sites in the attachment G glycoprotein. J Virol 2004; 78: 4675-83.
7. Blanc A, Delfraro A, Frabasile S and Arbiza J. Genotypes of respiratory syncytial vi rus group B iden ti fi ed in Uru gua y. Ar ch Vi rol 2004; 150: 603 -9 .
8. Henrickson K, Hall C. Diagnostic assays for respiratory syncytial virus disease. PedInf Dis J 2007; 26: S36- S40.
V Jornadas para Especialistas
Mini-simposio: Novedades en Virus Respiratoro Sincicial
El virus respiratorio sincicial (VRS) pertenece al género
Pneumovirus de la subfamilia Pneumovirinae de la familiaParamixoviridae(1). Al igual que los otros miembros de esta
familia, como el metapneumovirus humano, mide entre 100y 300 _m y posee un manto - bicapa lipídica que deriva dela membrana citoplasmática de la célula huésped- que recubre
una cápsula de simetría helicoidal. Esta contiene al genoma viral constituido por una hebra de ARN lineal de polaridadnegativa de 15,2 kb de longitud, que codifica para 10 proteínas.Entre ellas se encuentran las glicoproteínas (gp) F y G que forman las espículas(1) que sobresalen del manto; la proteínahidrofóbica pequeña no glicosilada -SH- de funcióndesconocida; las proteínas no glicosiladas M (28 kDa) y M2(22 kDa) que constituyen la capa proteica entre la cápsula yel manto, denominada matriz viral; la nucleoproteína N, la fosfoproteína P y la polimerasa L que conforman la cápsula
del virus y se asocian al ARN genómico, y dos proteínas noestructurales - NS1 (15 kDa) y NS2 (14 kDa), capaces deinhibir la acción del interferón, presentes en muy pequeñacantidad en los viriones, pero que se acumulan en las célulasinfectadas(1).
La proteína de fusión F es muy conservada entre las distintascepas de VRS(1), siendo fundamental para el ingreso del virusa la célula y su diseminación entre ellas al fusionar lasmembranas, determinando los característicos sincicios (célulasgigantes multinucleadas) de esta infección. La proteína Gparticipa en la unión al receptor celular y varía entre los VRS,especialmente en su porción extracelular (2). Existe sólo un
serotipo de VRS, aunque a nivel antigénico y genético sediferencian dos grupos virales, A y B (1,2), principalmente en
base a los cambios en la proteína G. Asimismo, dentro decada grupo existen variantes virales identificadas por distintosmétodos, como la digestión enzimática de los genes N y G,obteniéndose patrones de restricción (NP1-11)(3), y por losanálisis filogenéticos de la secuencia nucleotídica del gen dela gpG, estableciéndose genotipos virales. Se han definido 8genotipos (GA1-GA5) entre los VRS del grupo A y 10genotipos (GB1-GB4, URU1, URU2, BA) entre los B(4-7).
Los genotipos están diseminados en el mundo y en cadaepidemia se detecta la presencia simultánea de varios deellos, tanto del grupo A como del B, en proporciones variables
según la estación, el área geográfica y el año (1). Por otra parte,se ha tratado de relacionar el genotipo viral con la gravedadde la enfermedad por VRS, pero los resultados han sido
contradictorios.El diagnóstico de laboratorio de una infección por VRS se
puede realizar mediante diversos procedimientos. Existen técnicas rápidas como la detección de antígenos virales porinmunofluorescencia (IF), por ensayo inmunoenzimático(ELISA) e inmunocromatografía, fáciles de utilizar, de mayordisponibilidad y de bajo costo, pero de menor sensibilidadque el aislamiento viral, considerado el método de referencia.Los requerimientos técnicos, el rendimiento y la demora enel resultado del aislamiento limitan su uso, por lo que estásiendo reemplazado por la amplificación del genoma viralmediante transcripción reversa y reacción en cadena de lapolimerasa (RT-PCR), técnica de mayor sensibilidad,
especificidad y rapidez, por lo que es de elección especialmenteen el estudio de muestras de adultos. Sin embargo, aún estárestringida su utilización masiva por el costo del examen y lanecesidad de infraestructura y personal especializado(8). Elestudio serológico permite detectar los tipos de anticuerposdirigidos contra distintas proteínas del VRS(1), pero no es deutilidad clínica.

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 32/54
disponible en http://www.neumologia-pediatr ica.cl
NEUMOLOGIA PEDIATRICA ISSN 0718-3321
Mecanismo de infección y relación entre bronquitis y asma: ¿Anticuerpos monoclonales más alládel prematuro?Dr. Octavio RamiloDivisión of Pediatric Infectious DiseasesUT Southwestern Medical Center and Children’s Medical Center Dallas
172
El virus respiratorio sincicial (VRS) es uno de los agentes
infecciosos con mayor importancia en la población pediátrica.
Estudios realizados en la última década han demostrado que
el VRS es el principal patógeno que afecta a lactantes y niños
pequeños, y la causa más frecuente de hospitalización en
este grupo de edad. Estudios epidemiológicos efectuados
en distintas partes el mundo han confirmado su distribuciónuniversal. Hasta hace pocos años, la atención de los expertos
se focalizaba únicamente en la morbilidad y mortalidad asociada
a las infecciones agudas, sobretodo del tracto respiratorio
inferior en forma de bronquiolitis. Sin embargo, trabajos
prospectivos más recientes han demostrado una clara asocia-
ción entre la bronquiolitis por VRS y el riesgo subsiguiente
de padecer sibilancias de repetición o asma.
El VRS es un virus ARN, de cadena única y ordenada en
sentido inverso. Su genoma esta constituido por 10 genes y
codifica 11 proteínas. Pese a esta aparente simplicidad, este
virus ARN explota de forma muy eficaz su limitado número
de genes para poner en marcha mecanismos immunopato-génicos complejos y multifacéticos que le permiten escapar
del control del sistema inmune del huésped.
Su capacidad para alterar la respuesta inmune es evidente
y se refleja en su habilidad para ocasionar infecciones severas
en los lactantes e infecciones de repetición en todos los
grupos de edad, evitando el desarrollo de una respuesta
inmune eficaz y protectora, así como en su tendencia a
ocasionar morbilidad respiratoria crónica.
La complejidad de los mecanismos immunopatogénicos
implicados en las infecciones por VRS fue evidente pocos
años después de su descubrimiento en el año 1956. Los
intentos iniciales de desarrollar un vacuna se vieron frustrados
por la falta de eficacia y los marcados efectos adversos
documentados en los lactantes vacunados y expuestos al VRS
durante el siguiente brote epidémico.
Este fracaso inicial retrasó los esfuerzos de investigación y
la posibilidad de desarrollar vacunas eficaces, a la vez que
creó escepticismo y confusión acerca de la función de los
anticuerpos dirigidos contra el virus. A esta falta de progreso
en el desarrollo de immunoterapias, se unió el limitado éxito
para desarrollar fármacos antivirales eficaces o medidas
terapéuticas dirig idas a controlar la inflamación del tracto
respiratorio y los síntomas de la bronquiolitis.
Es importante recordar, especialmente a nuestros com-
pañeros más jóvenes, que este era el panorama, un tanto
desalentador con que nos encontrábamos hace solo 15 años.
La aparición de métodos de laboratorio para medir los
anticuerpos neutralizantes contra el VRS permitió iniciar una
nueva era en la desarrollo de immunoterapias dirigidas contra
este virus.
Estos métodos permitieron distinguir los anticuerpos anti-
VRS neutralizantes y con papel beneficioso, de anticuerpos
sin capacidad de neutralizar este virus. Usando esta tecnología
se pudieron seleccionar donantes adecuados con anticuerpos
neutralizantes anti-VRS y obtener las primeras preparaciones
policlonales de inmunoglobulina intravenosa con altos títulos
de anticuerpos neutralizantes contra el VRS, conocida como
RSV-IVIG (o Respigam).
Utilizando esta preparación policlonal de inmunoglobulina
se realizaron los estudios iniciales, randomizados que demos-
traron la eficacia de esta inmunoglobulina, RSV-IVIG, para
disminuir las infecciones respiratorias graves por VRS causantes
de hospitalización en lactantes prematuros o con enfermedad
pulmonar crónica. Aunque estos trabajos demostraron la
validez de este enfoque terapéutico, la administración de la
preparación policlonal de RSV-IVIG tenía problemas en la
práctica clínica debido a la necesidad de establecer acceso
intravenoso, el volumen de la solución y el tiempo necesario
para su administración.
Estos inconvenientes impulsaron el desarrollo de moléculas
más potentes, fundamentalmente anticuerpos monoclonales
neutralizantes dirigidos contra el VRS. De este grupo de
anticuerpos, solo uno, palivizumab, demostró una clara eficacia
clínica disminuyendo las hospitalizaciones debidas a infecciones
por VRS en niños prematuros y con enfermedad pulmonar
crónica. Es importante recordar que la aprobación de palivi-
zumab supuso un hito histórico, ya que es el primer anticuerpo
monoclonal aprobado para prevenir una enfermedad infec-
ciosa, y además en el grupo edad pediátrica y en los niños
más vulnerables.
Estudios randomizados posteriores demostraron la eficacia
de palivizumab en la prevención de infecciones graves por
VRS en niños con cardiopatías congénitas hemodinámicamente
significativas. Publicaciones subsiguientes han confirmado estos
hallazgos iniciales en diferentes países y aquí es justo destacar

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 33/54
173Mecanismo de infección y relación entre bronquitis y asma ¿Anticuerpos monoclonales más allá del prematuro?
el papel fundamental, reconocido internacionalmente, des-
empeñado por los investigadores españoles.
Sin embargo la potencial utilidad terapéutica de palivizumab
no se limita a estas tradicionales poblaciones de riesgo bien
caracterizadas. Además de los grupos de riesgo clásicos,
existen otros grupos de pacientes que claramente se pueden
beneficiar de profilaxis con anticuerpos anti-VRS, como los
pacientes con enfermedades pulmonares severas como la
fibrosis quística, pacientes con afectaciones neurológicas y
neuromusculares importantes, pacientes con terapia immu-
nosupresora debido a transplantes de órganos sólidos o de
médula ósea. Incluso existe una limitada experiencia adminis-
trando este anticuerpo en forma de tratamiento en casos de
infección VRS ya establecida en pacientes de alto riesgo. Sin
embargo, es importante dejar claro que en estas otras
poblaciones no tradicionales la experiencia es limitada, ya que
desde un punto de vista práctico los números de pacientes
impiden realizar estudios randomizados controlados.
Además de la morbilidad aguda causada por las infeccionespor VRS, estudios epidemiológicos y experimentales realizados
en los últimos años han confirmado la capacidad de este virus
para causar patología pulmonar crónica, manifestada funda-
mentalmente en forma de sibilancias recurrentes que pueden
ocurrir hasta una década después de la infección aguda.
Estudios experimentales han demostrado que la administración
de anticuerpos anti-VRS disminuyó no solo la patología aguda
sino también las secuelas pulmonares crónicas causadas por
el VRS.
Muy recientemente, un estudio caso-control, multinacional
ha demostrado que niños prematuros sin enfermedad pul-
monar crónica que recibieron profilaxis con palivizumab tuvieron disminución significativa de sibilancias recurrentes
comparados con niños control que no recibieron profilaxis.
Pese a ciertas limitaciones, este es un estudio fundamental ya
que por primera vez establece el principio que intervenciones
terapéuticas dirigidas contra el VRS pueden disminuir las
secuelas pulmonares posteriores.
A partir de paliv izumab se ha desarrol lado un anticuerpo
de mayor potencia también dirigido contra la proteína F del
VRS. Este nuevo anticuerpo, motavizumab, ha demostrado
clara eficacia disminuyendo las hospitalizaciones por bron-
quiolitis causadas por VRS en prematuros. Sin embargo su
mayor potencia sugiere la posibilidad de utilizarlo en otrassituaciones clínicas complejas y con otras poblaciones de
pacientes más allá de las tradicionales poblaciones de riesgo.
LECTURAS RECOMENDADAS
1. Collins PL, E. J. Crowe. Respiratory syncytial virus and metapneumovirus. In: KnipeDM, ed. Fields Virology. Philadelphia: Lippincott Williams & Wilkins; 2007:1601-46.
2. Hall CB M, C.A. Respiratory Syncytial Virus. . Mandell:Principles and Practice ofInfectious Diseases. 5 ed: Churchill Livingstone, Inc.; 2000.
3. Shay DK, Holman RC, Newman RD, Liu LL, Stout JW, Anderson LJ. Bronchiolitis-associated hospitalizations among US children, 1980-1996. Jama 1999; 282: 1440-6.
4. Sigurs N, Gustafsson PM, Bjarnason R, et al. Severe respiratory syncytial virusbronchiolitis in infancy and asthma and allergy at age 13. Am J Respir Crit CareMed 2005; 171: 137-41.
5. Stein RT, Sherrill D, Morgan WJ, et al. Respiratory syncytial virus in early life andrisk of wheeze and allergy by age 13 years. Lancet 1999; 354: 541-5.
6. Buckingham SC, Jafri HS, Bush AJ, et al. A randomized, double-blind, placebo-controlled trial of dexamethasone in severe respiratory syncytial virus (RSV) infection:effects on RSV quantity and clinical outcome. J Infect Dis 2002; 185: 1222-8.
7. Malley R, DeVincenzo J, Ramilo O, et al. Reduction of respiratory syncytial virus
(RSV) in tracheal aspirates in intubated infants by use of humanized monoclonalantibody to RSV F protein. J Infect Dis 1998; 178: 1555-61.
8. Jafri HS, Chavez-Bueno S, Mejias A, et al. Respiratory syncytial virus inducespneumonia, cytokine response, airway obstruction, and chronic inflammatoryinfiltrates associated with long-term airway hyperresponsiveness in mice. J InfectDis 2004; 189: 1856-65.
9. Reduction of respiratory syncytial virus hospitalizat ion among premature infantsand infants with bronchopulmonary dysplasia using respiratory syncytial virusimmune globulin prophylaxis. The PREVENT Study Group. Pediatrics 1997; 99:93-9.
10. Feltes TF, Cabalka AK, Meissner HC, e t al. Palivizumab prophylaxis reduceshospitalization due to respiratory syncytial virus in young children withhemodynamically significant congenital heart disease. J Pediatr 2003; 143: 532-40.
11. Palivizumab, a humanized respiratory syncytial virus monoclonal antibody, reduceshospitalization from respiratory syncytial virus infection in high-risk infants. TheIMpact-RSV Study Group. Pediatr ics 1998; 102 (3 Pt 1): 531-7.
12. Mejias A, Chavez-Bueno S, Rios AM, et al. Anti-respiratory syncytial virus (RSV)neutralizing antibody decreases lung inflammation, airway obstruction, and airwayhyperresponsiveness in a murine RSV model. Antimicrob Agents Chemother 2004;
48: 1811-22.13. Mejias A, Chavez-Bueno S, Rios AM, et al. Comparative effects of two neutralizing
anti-respiratory syncytial virus (RSV) monoclonal antibodies in the RSV murinemodel: time versus potency. Antimicrob Agents Chemother 2005; 49: 4700-7.
14. Simoes EA, Groothuis JR, Carbonell-Estrany X, et al. Palivizumab prophylaxis,respiratory syncytial virus, and subsequent recurrent wheezing. J Pediatr 2007;151: 34-42, e1.

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 34/54
disponible en http://www.neumologia-pediatr ica.cl174
NEUMOLOGIA PEDIATRICA ISSN 0718-3321
Patrón epidemiológico en Chile y el mundoDr. Luis Fidel AvendañoPediatra InfectólogoHospital San Borja Arriarán
Se reconoce que el 50-68% de los niños se infectan con virus respiratorio sincicial (VRS) durante el primer año de viday al segundo cumpleaños virtualmente todos se han contagiado.La tasa de ataque depende de la exposición y de la inmunidadprevia: en salas cunas se contagia el 98% de los expuestospor primera vez. En la patogenia de la infección por VRSparticipan factores dependientes del virus, del ambiente y delhuésped.
El ambiente: El VRS tiende a presentase en brotes,dependiendo de condiciones geográficas: temperatura,
humedad, contaminación aérea, concentración y característicasde la población. El VRS puede mantenerse viable en climas fríos y calientes, secos y húmedos. El VRS puede permanecer viable por 6 horas o más en el ambiente, dependiendo deciertas condiciones. Existe controversia sobre la influencia dela contaminación aérea en la gravedad de la enfermedad. Elmayor impacto en salud coincide con la epidemia de VRS.La concentración de la población implica mayor riesgo decontagio, no necesariamente de más gravedad: ¿hay selecciónde lactantes de más riesgo?
El virus: Las cepas de VRS circulantes localmente y en elmundo se pueden clasificar y caracterizar usando la tecnología
actualmente disponible: grupos A y B (IFI), lineajes (RFLP) ygenotipos (secuenciación gpG). Los grupos A y B circulan juntos o se alternan, predominando el A; no hay clara relacióncon gravedad; los años en que circula una buena cantidad de VRS-B las epidemias son más precoces, bruscas y “molestosas”.Los distintos lineajes y genotipos muestran variacionesgeográficas y temporales: circulan diversas cepas durante una temporada y en diversas partes del mundo a veces circulanlas mismas cepas. Podrían explicar variaciones en la forma depresentación de las epidemias, por eventuales presionesselectivas. No habría una cepa más transmisible o más virulenta.
LECTURAS RECOMENDADAS
1. Avendaño LF, Palomino MA, Larrañaga C. Surveillance for Respiratory Syncytial Virus in Infants Hospitalized for Acute Lower Respiratory Infection in Chile (1989 to 2000). J Clin Microbiol 2003; 41: 4879-4882.
2. Avendaño LF, Parra J, Padilla C, Palomino MA. Impacto en salud infantil del invierno2002: disociación entre factores ambientales y virus respiratorio sincicial, enSantiago. Rev Méd Chile 2003; 131: 902-908.
3. Cane P. Molecular epidemiology of respiratory syncytial virus. Rev. Med. Virol 2001;11: 103-116.
4. Falsey AR. Respiratory Syncytial Virus infection in adults. Sem Resp Crit Care Med2007; 28: 171-181.
5. Girardi B, Astudillo O, Zúñiga F. El programa IRA en Chile: hitos e historia. RevChil Pediatr 2001; 72: 292-300.
6. Hall CB, Walsh EE, Schnabel KC, et al. Occurrences of Groups A and B ofRespiratory Syncytial Virus over 15 Years: Associated Epidemiologic and ClinicalCharacteristics in Hospitalized and Ambulatory Children. J Infect Dis 1990; 162:1283-1290.
7. Hall CB. Respiratory Syncytial Virus and Parainfluenza Virus. N Engl J Med 2001;334: 1917-1928.
8. Peret TC, Hall CB, Hammond GH, et al. Circulation patterns of Group A and BHuman Respiratory Syncytial Virus Genotypes in 5 Communities in North América. J Infect Dis 2000; 181: 1891-1896.
9. Sullender WM. Respiratory Syncytial Virus Genetic and antigenic Diversity. ClinMicrobiol Rev 2000; 13: 1-15.
10. Yusuf S, Piedimonte G, Auais A, et al. The Relationship of Meteorological Conditions to the Epidemic Activity of Respiratory Syncytial Virus. Epidemiol Infect 2007; 135:1077-90.

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 35/54
175
Dr. Pablo Bertrand
Pediatra Broncopulmonar Hospital Clínico Universidad Católica
NEUMOLOGIA PEDIATRICA ISSN 0718-3321
Manejo clínico del paciente hospitalizado por VRS:Rol de los antiinflamatorios
disponible en http://www.neumologia-pediatrica.cl
La infección por virus respiratorio sincicial (VRS) es la causamás importante de hospitalización en niños menores de dosaños. En nuestro país anualmente se registran cerca de 3000hospitalizaciones en la temporada invernal, lo que constituyeun desafío para nuestra situación hospitalaria. Esta situaciónse ve empeorada debido a que la infección por VRS noproduce inmunidad adecuada y por tanto la reinfección esun hecho común.
Aunque la fisiopatología de la bronquiolitis por VRS se haestudiado en forma exhaustiva, y se ha reconocido como fenómeno importante la presencia de inflamación de la víaaérea, no existe claridad de cuales serían los mecanismosmás importantes en este proceso. Se ha descrito la importanciaque podría tener la infección por VRS en gatillar inflamaciónde tipo “neutrofÍlica” a diferencia de la “eosinofÍlica”, carac- terística del asma. Esto ha motivado a muchos investigadoresen el mundo a buscar aquellos mediadores que pudieran jugar un rol protagónico en la etapa aguda de la infección,pero todavía no existe claridad al respecto.
El tratamiento de la bronquiolitis por VRS del niño hospita-
lizado se ha orientado a detener la progresión de los hallazgospatológicos que ocurre en la vía aérea, es decir, obstrucciónbronquial e inflamación principalmente. La utilidad de losantiinflamatorios (corticoesteroides) ha sido objeto de grancontroversia. Inicialmente, los resultados de los corticoeste-roides en bronquiolitis por VRS en animales fueron muyoptimistas, corroborando la importancia de la inflamación eneste modelo. Sin embargo, la mayoría de los estudios realizadosen humanos no han logrado demostrar utilidad de los corti-coesteroides sistémicos en la fase aguda de bronquiolitis por VRS.
Estudios de metanálisis realizados en este tiempo muestran
resultados contradictorios. En un metanálisis realizado porGarrison y colaboradores se ejecutó una búsqueda de todoslos estudios que comparaban corticoesteroides y placebo enla fase aguda de bronquiolitis. Se seleccionaron 5 estudios (n:347 pacientes) cuyos principales indicadores fueron: estadíaen el hospital, días con síntomas y puntaje clínico.
El análisis final concluye que existe una diferencia favorablede -0.43 días en el grupo tratado comparado con el placeboque resulta ser significativo. Sin embargo, uno de los estudios,incluyó pacientes de mayor gravedad (ventilación mecánica)cuyas estadías se escapaban claramente del promedio debronquiolitis, y que produjeron una desviación importantede los días de estadía en el hospital. Este estudio pudiera
justificar el uso de esta droga en pacientes graves en UCI,donde puede tener mayor indicación, cosa que los autoresdiscuten en forma bastante clara, pero no justifica su utilizaciónen los demás pacientes hospitalizados. En el análisis desubgrupos no fue posible encontrar estas diferencias en díasde hospitalización.
En la revisión Chocrane realizada por Patel y colaboradoresse llevó a cabo una nueva selección de 13 estudios (n:1198)que compararon placebo y corticoesteroides y se encontróla misma diferencia que en el metanálisis previo, pero sinalcanzar poder estadístico. Esta revisión presenta un númeromayor de pacientes y en el análisis de subgrupos (menoresde 12 meses, pacientes con bronquiolitis sólo VRS y primerepisodio de sibilancias) las comparaciones tampoco alcanzaronpoder estadístico. En conclusión, el uso de corticoesteroides tiene escaso fundamento como tratamiento de rutina parala bronquiolitis por VRS y la excepción la constituye la formagrave de manejo en UTI con ventilación mecánica.
En esta misma línea de tratamiento antiinflamatorio se hainvestigado el rol que presentan las citoquinas proinflamatoriasy los leucotrienos en bronquiolitis por VRS. En un estudiorealizado por Bisgaard, se insinúa una potencial respuesta al tratamiento con el uso de montelukast (inhibidor de leuco- trienos) en pacientes menores de 30 meses con su primerepisodio de bronquiolitis por VRS. En este estudio el síntoma tos presentó una significativa mejoría en el grupo tratado versus el con placebo, pero no hubo diferencias en otrosparámetros clínicos. Esta respuesta se intentó validar a travésde un estudio multicéntrico cuyo principal parámetro demedición fue estadía en el hospital, sin embargo los resultadosde este estudio no se han dado a conocer en forma oficial.De momento no es posible concluir que los inhibidores de
leucotrienos sean una alternativa terapéutica en bronquiolitispor VRS.
Recientemente se ha estudiado la importancia de superóxi-dos en la inflamación de células epiteliales por VRS y elbloqueo de señales de transducción por medio del uso deantioxidantes como posibles mediadores importantes en lainflamación de bronquiolitis VRS. Con esta idea se realizó unestudio en modelo animal donde se encontró que la situaciónde productos de peroxidación lipídica se altera en aquellosratones expuestos a la enfermedad por VRS, y que el uso deantioxidantes logró disminuir la gravedad clínica de aquellosprotegidos y disminuyó las citoquinas mediadoras de infeccióny daño pulmonar agudo. Frente a estos resultados nuevamente

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 36/54
LECTURAS RECOMENDADAS
1. Panitch HB. Bronchiolit is in infants. Curr Opin Pediatr 2001; 13: 256-60.2. Roosvelt G, Sheehan K, Grupp-Phelan J, Tanz RR, Listernick R. Dexamethasone
in bronchiolitis: a randomized controlled trial. Lancet 1996; 348: 292-295.3. Labbe A. Treatment of acute bronchiolitis in infants. Role of bronchodilators and
steroids. Arch Pediatr 1996; 3: 383-9.4. Berger I, Argaman Z, Schwartz SB et al. Efficacy of corticosteroids in acute
bronchiolitis: short-term and long-term follow-up. Pediatr Pulmonol 1998; 26:162-6.
5. Barbeu JU, Robertson CF, Robinson PJ. Implementation of evidence-basedmanagement of acute bronchiolitis. J Pediatr Child Health 2000; 36: 491-7.
6. King V. Pharmacologic Treatment of Bronchiolitis in Infants and Children. A systematicReview. Arch Pediatr Adolesc Med. 2004; 158: 127-137.
7. Steiner R Treating Acute Bronchiolitis Associated with RSV. Am Fam Physician 2004;69: 325-30.
8. Garrison MM, Christakis DA, Harvey E, Cummings P and Davis RL. SystemicCorticosteroids in Infant Bronchiolitis: A Meta-analysis. Pediatrics 2000; 105: XX
9. Patel H, Platt R, Lozano JM, Wang EE. Glucocorticoids for acute viral bronchiolitisin infants and young children. Cochrane Database Syst Rev 2004; (3): CD004878.
10. Bisgaard H. A randomized trial of montelukast in respiratory syncytial viruspostbronchiolitis. Am J Respir Crit Care Med 2003; 167:379-83.
11. Castro SM, Guerrero-Plata A, Suarez-Real G et al. Antioxidant Treatment AmelioratesRespiratory Syncytial Virus-induced Disease and Lung Inflammation. Am J RespirCrit Care Med 2006; 174: 1361-1369.
12. Black CP Systematic review of the biology and medical management of respiratorysyncytial virus infection. Respir Care 2003; 48: 209-31.
Manejo clínico del paciente hospitalizado por VRS: Rol de los antiinflamatorios176
debemos tener cautela por cuanto en la infección por VRSel comportamiento del humano no necesariamente es reflejode los modelos animales.
En resumen, los avances recientes permiten entendermejor el panorama respecto de los mecanismos en inflamacióninvolucrados en bronquiolitis, pero no han logrado ofrecer
un tratamiento farmacológico específico que tenga resultadossignificativos en la práctica clínica.

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 37/54

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 38/54
178 Infección respiratoria baja por VRS: Mitos y realidades
lización alcanza la zona periférica en lactantes con bronquiolitis.De acuerdo a esto los B2 deberían administrarse en aerosolessuperfinos.
Dos publicaciones recientes muestran el éxito del uso desolución salina al 3% y epinefrina. Quizás lo más relevantede estos estudios, es que el método de administración, fue
con un sistema que genera un aerosol con partículas de 1micrón de masa media. Por último el uso del BIPAP aparececomo una alternativa de tratamiento eficaz incluso en pacientescon hipercapnia, lo que hace pensar que su uso mas precozpude evitar la progresión a situaciones de mayor gravedad.Es posible que ambas posiciones, llevadas a su extremo, tratary no tratar, tengan mitos y que la realidad esté en lo queobservamos en nuestros pacientes.
LECTURAS RECOMENDADAS
1. Brandenburg AH, Jeannet PY, Steensel-Moll HA, et al. Local variabili ty in respiratorysyncytial virus disease severity. Arch Dis Child 1997; 77: 410-4.2. López Guinea A, Casado Flores J, Martín Sobrino MA, et al. Severe bronchiolitis:
Epidemiology and clinical course of 284 patients. An Pediatr (Barc) 2007; 67: 116-22.
3. Ségala C, Poizeau D, Mesbah M, Willems S, Maidenberg M. Winter air pollutionand infant bronchiolit is in Par is. Environ Res 2008;106: 96-100.
4. De Vincenzo JP, El Saleeby CM, Bush AJ. Respiratory syncytial virus load predictsdisease severity in previously healthy infants. J Infect Dis 2005; 191: 1861-8.
5. Johnson JE. The histopathology of fatal untreated human respiratory syncytial virusinfection. Mod Pathol 2007; 20: 108-19.
6. Tulic MK, Hurrelbrink RJ, Prêle CM, Laing IA, Upham JW, Le Souef P, Sly PD, HoltPG. TLR4 polymorphisms mediate impaired responses to respiratory syncytial virus and lipopolysaccharide. J Immunol 2007; 179: 132-40.
7. Hammer J, Numa A, Newth CJ, et al. Immunopathogenesis of respiratory syncytial virus bronchio litis. Acute respiratory distress syndrome caused by respiratorysyncytial virus. Pediatr Pulmonol 1997; 23: 176-83.
8. Tibby SM, Hatherill M, Wright SM, et al. Exogenous surfactant supplementationin infants with respiratory syncytial virus bronchiolitis. Am J Respir Crit Care Med
2000; 162 (4 Pt 1): 1251-6.9. Merkus PJ, de Hoog M, van Gent R, de Jongste JC. DNase treatment for atelectasis
in infants with severe respiratory syncytial virus bronchiolitis. Eur Respir J 2001;18: 734-7.
10. Modl M, Eber E, Weinhandl E, Gruber W, Zach MS. Assessment of bronchodilatorresponsiveness in infants with bronchiolitis. A comparison of the tidal and the raised volume rapid thoracoabdominal compression technique. Am J Resp ir Crit CareMed 2000; 161(3 Pt 1): 763-8.
11. Rao X, Liu X, Jiang Q, Jiao A, Jiang Y. Pulmonary function in infants with respiratorysyncytial virus bronchiolitis. Zhonghua Yi Xue Za Zhi 2002; 82: 182-5.
12. van Woensel JB, van Aalderen WM, de Weerd W, et al. Dexamethasone for treatment of patients mechanically ventilated for lower respiratory tract infectioncaused by respiratory syncytia l virus. Thorax 2003; 58: 383-7.
13. Kuyucu S, Unal S, Kuyucu N, Yilgor E. Additive effects of dexamethasone innebulized salbutamol or L-epinephrine treated infants with acute bronchiolitis.Pediatr Int 2004; 46: 539-44.
14. Hammer J, Numa A, Newth CJ. Albuterol responsiveness in infants with respiratory failure caused by respiratory syncytial virus infection. J Pediatr 1995; 127: 485-90.
15. Gómez-y-López RE, Hernández-Sierra JF, Torres-Ruvalcaba BA, et al. Comparative
clinical study of dexamethasone vs. nebulized salbutamol in acute bronchiolitis. GacMed Mex 2007; 143: 189-92.
16. Sánchez I, Vizcaya C, García D, Campos E. Response to bronchodilator in infants with bronchiolitis can be predic ted from wheeze characteristi cs. Respiro logy2005;10: 603-8.
17. Modl M, Eber E, Malle-Scheid D, Weinhandl E, Zach MS. Does bronchodilatorresponsiveness in infants with bronchiolitis depend on age? J Pediatr 2005; 147:617-21.
18. Mallory GB Jr, Motoyama EK, Koumbourlis AC, Mutich RL, Nakayama DK. Bronchialreactivity in infants in acute respiratory failure with viral bronchiolitis. Pediatr Pulmonol1989; 6: 253-9.
19. Soto ME, Sly PD, Uren E, Taussig LM, Landau LI.Bronchodilator response duringacute viral bronchiolitis in infancy. Pediatr Pulmonol 1985; 1: 85-90.
20. Wildhaber JH, Dore ND, Devadason SG, Hall GL, Hamacher J, Arheden L,LeSouëf PN. Comparison of subjective and objective measures in recurrently wheezy infants. Respiration 2002; 69: 397-405.
21. Kuzik BA, Al-Qadhi SA, Kent S, Flavin MP, Hopman W, Hotte S, Gander S. Nebulizedhypertonic saline in the treatment of viral bronchiolitis in infants. J Pediatr 2007;151: 235-7.
22. Tal G, Cesar K, Oron A, Houri S, Ballin A, Mandelberg A. Hypertonicsaline/epinephrine treatment in hospitalized infants with viral bronchiolitis reduceshospitalization stay: 2 years experience. Isr Med Assoc J 2006; 8: 169-73.
23. Amirav I, Balanov I, Gorenberg M, et al. Beta-agonist aerosol distribution inrespiratory syncytial virus bronchiolitis in infants. J Nucl Med 2002; 43: 487-91.

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 39/54
Dr. Pedro AstudilloNeumólogo Pediatra
Jefe Unidad de Salud Respiratoria, Ministerio de Salud Jefe Servicio de Pediatría, clínica INDISA
NEUMOLOGIA PEDIATRICA ISSN 0718-3321
Manejo epidemiológico de los brotes de VRS
disponible en http://www.neumologia-pediatr ica.cl 179
Las enfermedades respiratorias constituyen la causa másimportante de hospitalización en menores de 5 años (35,4%en 2004). De ellas, destacan las infecciones virales, especial-mente el virus respiratorio sincicial (VRS), que representa las tres cuartas partes de los hallazgos de virus respiratorios enChile. Se estima que 240.000 niños menores de 2 años seinfectan con VRS cada año, requiriendo hospitalización aproxi-madamente el 2% de ellos (± 4800 egresos), situación quese presenta en forma estacional en los meses de invierno,
período en el que los virus concurren junto a otros factoresde riesgo como el frío y la contaminación atmosférica.
El VRS se presenta en brotes epidémicos, cuyo peakcoincide cada año exactamente con el más alto nivel dehospitalizaciones pediátricas. Durante este período, se tensionaal máximo la red asistencial, en especial por el alto requeri-miento de camas hospitalarias en los Servicios de Pediatríade la región metropolitana. Anualmente se calcula que sehospitalizan aproximadamente 5.000 menores de 2 años porIRA baja debida a VRS en Chile.
Una alta proporción de estas hospitalizaciones ocurre enla región metropolitana. Dado que la mayor parte de dichas
hospitalizaciones ocurren en un plazo no mayor de 3 meses,se produce una gran demanda de camas, que sobrecarga y tensiona al sistema de salud, tanto público como privado.Durante el período peak de VRS, los ingresos diarios a camaspediátricas por causa respiratoria superan el número de 100en los hospitales de Santiago, habiéndose alcanzado la cifrarecord de 168 en un día, en julio de 2004.
CAMPAÑA DE INVIERNO
Para abordar este importante problema epidemiológico, elMinisterio de Salud desarrolla desde el año 1994 una estrategiadenominada “Campaña de Invierno”, destinada a focalizaresfuerzos en el período peak de enfermedades respiratorias.Esta estrategia tiene 2 vertientes fundamentales: a) una líneapreventiva y de comunicaciones, que incluye vacunaciónantiinfluenza y mensajes a la población a través de mediosmasivos, destinados a prevenir factores de riesgo y a reconocergravedad de las infecciones respiratorias, y b) un componenteasistencial, que consiste en el refuerzo estacional de todoslos niveles de atención, con el foco puesto en Servicios deUrgencia y sobre todo en camas hospitalarias, tanto básicascomo de cuidados críticos.
CRONOGRAMA DE LA CAMPAÑA DE INVIERNO
Cada año, la Campaña se inicia en el mes de enero con laelaboración de planes por parte de los Servicios de Salud,los que son evaluados a nivel del Ministerio por la Unidad deSalud Respiratoria, transfiriendo a los Servicios los recursosrequeridos para ejecutar dichos planes, en el marco delpresupuesto de la Campaña. Paralelamente, se elaboranescenarios epidemiológicos predictivos sobre la probablesituación que afectará al país; estos escenarios se construyen
sobre la base de los antecedentes epidemiológicos de losaños anteriores en el país, la información del invierno delhemisferio norte y las probables condiciones de temperatura,pluviometría y contaminación del próximo otoño-invierno.Estos escenarios se discuten con el Subsecretario de Redes Asistenciales, a fin de implementar las medidas necesariaspara hacerles frente.
En el mes de marzo, se inicia la vacunación antiinfluenza,que normalmente alcanza alta cobertura en los grupos deriesgo. En la parte asistencial, los meses de abril a junio secaracterizan por una fuerte demanda asistencial ambulatoria, traducida en una gran sobrecarga en atención primaria y
Servicios de Urgencia. Esta alta demanda ambulatoria, sedebe a la circulación de virus influenza. Posteriormente,generalmente a contar de la 2ª quincena de junio, se iniciael brote anual de VRS, debiendo adaptarse toda la redhospitalaria pediátrica para pacientes respiratorios, suspen-diéndose la cirugía electiva e implementando todas las camascon oxígeno. Esta reconversión de camas también ocurre enlas unidades paciente crítico. Esta transformación de loshospitales pediátricos y Servicios de Pediatría en hospitalesrespiratorios es una estrategia única, que no tiene reportesen otros lugares del mundo y ocurre generalmente hasta fines del mes de agosto, período en que toda la red asistencial vuelve a la normalidad.
Todo el esfuerzo asistencial es apoyado simultáneamentepor la campaña de comunicaciones. Permanentemente, desdesu inicio, la Campaña de Invierno es apoyada por un completosistema de vigilancia epidemiológica, que permite anticipar,con una antelación de 1 a 2 semanas, los momentos clavesde la Campaña, permitiendo organizar y gestionar óptima-mente la red asistencial.
PRINCIPALES RESULTADOS
Desde hace varios años, todos los niños que requierenhospitalización en el marco de la Campaña de Invierno, logranser hospitalizados, aunque en el período de alta demanda,

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 40/54
180 Manejo epidemiológico de los brotes de VRS
LECTURAS RECOMENDADAS
1. Mallol J, Barrueto L, Girardi G, et al: Bronchodilator effect of fenoterol andipatropium bromide in infants with acute wheezing: use of MDI with a spacerdevicer. Pediatr Pulmonol 1987; 3: 352.
2. Abara S, Girardi G, Muñoz R: Manejo del síndrome bronquial obstructivo agudodel lactante en una sala de pre-hospitalización. Enf Respir y Cir Torác 1990; 6:192-97.
3. Astudillo P, Mancilla P, Girardi G, Aranda C, Gamboa R: Hospitalización abreviadaen atención primaria de salud. Rev Chil Enf Resp 8 (supl); 262.
4. Girardi G, Astudillo P: Tratamiento ambulatorio del síndrome de obstrucciónbronquial. Texto Pediatría. Meneghello V Edición. Tomo 1. 1351-1354.
5. Pavon D, Castro-Rodriguez JA, Rubilar L, Girardi G: Relation Between PulseOximetry and Clinical Score in Children whit Acute Wheezing Less Than 24 Monthsof Age. Pediatr Pulmonol 1999; 27: 423-7.
6. Girardi G, Astudillo P, Mancilla P, Gamboa R, Risopatrón F: Enfoques innovadoresen atención primaria en Chile. Rev Uruguaya de Atención Primaria 1993; 3: 2-10.
7. Girardi G, Astudillo P, Zúñiga F. El programa IRA en Chile: hitos e historia. Rev ChilPed 2001; 72: 292-300.
deben esperar, a veces horas, hasta acceder a una cama. Estoconduce al principal resultado de impacto, como es la caídade la mortalidad infantil por neumonía, desde una tasa de2.39 por 1000 RNV en 1990 a una de 0.19 por 1000 RNVen 2007, lo que significa una caída de 92.2%, constituyendoel mejor resultado sanitario de los últimos 20 años en Chile.

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 41/54
181
Dr. Francisco PradoPediatra Broncopulmonar Unidad Salud Respiratoria, Ministerio de SaludSubsecretaria de Redes
NEUMOLOGIA PEDIATRICA ISSN 0718-3321
Programa de profilaxis VRS en niños con displasiabroncopulmonar en Atención Primaria de Salud
disponible en http://www.neumologia-pediatrica.cl
DEFINICIÓN DEL PROBLEMA
Existe una alta proporción de enfermedades respiratoriasagudas bajas (IRAB) que motiva anualmente el establecimientode la Campaña de Invierno destinada a fortalecer las estrategiasresolutivas en la Red Asistencial.
Los pacientes más vulnerables son los extremos de la vida,
principalmente aquellos pacientes con enfermedades pulmo-nares crónicas, las cuales en la primera infancia, se relacionan fuertemente a secuelas respiratorias de la prematurez.
Este grupo de lactantes tiene mayor riesgo de requerircuidados especiales y monitorización permanente. Para esto,los pacientes deben ser ingresados a camas críticas, obligandoen muchos casos a altos costos por la necesidad de comprarservicios en clínicas privadas. Una estrategia de prevenciónespecífica permitiría mejorar los indicadores sanitarios y ahorraruna importante suma de recursos.
En nuestro país nacen anualmente (Anuario INE MINSAL2004) 259.069 niños. De ellos, alrededor de un 1% (2565)
son menores de 1500 g o tienen < de 32 semanas de edadgestacional, con una prevalencia variable de displasia bronco-pulmonar (DBP) de 20 a 60% en niños con PN de 1500 -1000 g o < de 1000 g respectivamente (Guías GES). Lanecesidad de oxigenoterapia prolongada (> 36 semanas ) es variable según el peso de nacimiento y puede ir desde el10% (1250 - 1500 g) al 35 % en < de 1000 g. De estosniños un 10% requiere oxigenoterapia ambulatoria duranteel primer año de vida. Todos ellos tienen cobertura por elPrograma Nacional de Oxigenoterapia Ambulatoria. Cercadel 50% de los pacientes se encuentra en la Región Metro-politana (Anexo A).
Los prematuros abordados en el Plan de Acceso Universalcon Garantías Explícitas (PN menor a 1500 g o menores de32 semanas de edad gestacional) corresponden a dos tiposde pacientes, primero aquellos con DBP sin oxigenoterapiaambulatoria y segundo, los niños con enfermedad pulmonarcrónica o DBP con oxigenoterapia ambulatoria. Este ultimogrupo tiene significativo mayor riesgo de desarrollar una porIRAB grave por Virus Respiratorio Sincicial (IRAB - VRS),siendo el grupo que concentra los mayores costos e impactosocial.
Estos dos grupos de lactantes prematuros tienen una alta tasa de readmisión durante los primeros 2 años de vida(50%), causada hasta en el 30% de los casos por IRAB -
VRS, obligando a hospitalizaciones no menores de 5 días enunidades pediátricas de cama crítica (UCIP/ Unidad deIntermedio), generalmente por insuficiencia respiratoria agudaque requieren ventilación mecánica invasiva en no menosdel 10% de los pacientes ingresados.
La ventilación mecánica invasiva tiene implícito el riesgo
secundario a establecer una vía aérea artificial (tubo endotra-queal) aumentando las posibilidades de infección intrahospi- talaria, daño secundario irreparable de la vía aérea (estenosissubglótica adquirida), daño pulmonar crónico y enfermedadpulmonar obstructiva. También es posible el daño cerebralpor hipoxia o apneas preferentemente en niños con injuriasanteriores. Todas estas condiciones limitan severamente enel niño la calidad de vida durante la infancia, posiblementeadolescencia y adultez.
Con relación al costo directo de estas hospitalizacionespara el sector público de salud, la Unidad de Respiratoria deMINSAL, estima que la hospitalización de los pacientespediátricos a los cuáles va dirigido este programa, considerandola frecuencia de días de estadía mencionados y valorizandosólo el día cama critica en Unidades de Cuidados Intensivos- UCI en $190.000 diarios tiene un costo mínimo de $1.000.000 en el sistema público. Los costos relacionados ala ventilación mecánica y otras prestaciones pueden elevarconsiderablemente esta cifra, más aún de ser necesariocomprar servicios en el extrasistema, situación posible enCampaña de Invierno.
Las desventajas que las hospitalizaciones por IRAB - VRSconllevan para estos pacientes, sus familias y para el sectorpúblico se resumen en:
• Mayor taza de hospitalización utilizando preferentementecamas críticas (Intensivo e Intermedio), fundamentalmentedurante la campaña de invierno.
• Mayor taza de mortalidad (> al 5%, para una tasareferencial no mayor del 1% de los hospitalizados sin factoresde riesgo ) y complicaciones pulmonares y extrapulmonares.
• Deterioro de la calidad de vida de estos niños y sus familias prolongando la condición de pacientes con enfermedadpulmonar crónica y requerimientos de tecnologías especialesen domicilio (oxigenoterapia ambulatoria, ventilación mecánicadomiciliaria) durante los primeros años de la infancia.
• Aumento del riesgo de morbimortalidad durante los 2

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 42/54
182
Tabla 1.- PREVENCIÓN DE LA INFECCIÓN POR VRSRecomendaciones AAP (American Academy of Pediatrics)
Prematuros Prematuros Prematuros Niños con DBP Niños con
≤28 semanas 29 a 32 semanas 32 a 35 semanas Cardiopatía Congénita
Hemodinámicamente
significativa
Hasta los 12 Hasta los 6 meses Hasta los 6 meses Hasta los 2 años, Hasta los 2 años
meses de edad de edad al inicio de edad al inicio en tratamiento último
estación VRS. estación VRS 6 meses con O2,
con 2 ó más broncodilatadores
factores de riesgo
adicionales
Programa de profilaxis VRS en niños con displasia broncopulmonar en Atención Primaria de Salud
primeros años de vida y aumento de la prevalencia de asmaen la primera infancia.
• Aumento de la presión social sobre el sistema público,por las familias, entorno y los medios de comunicación.
• Separación del niño y su familia con deterioro en sudesarrollo psicomotor y serios trastornos en la dinámica familiar y social.
• Aumento del costo social por perdida de años de vidaajustados por calidad (QALYS o quality-adjusted life years)
No obstante conocer que la principal causa de morbimor- talidad en estos niños altamente vulnerables se relaciona al VRS, actualmente sólo existe cobertura de inmunización
desde los primeros 2 meses de vida con vacuna conjugadaantineumocócica a seis valencias y vacuna antigripal en losmayores de 6 meses de edad. La cobertura con anticuerposmonoclonales anti VRS se encuentra disponible en nuestropaís desde hace varios años sin existir estudios disponiblesde costo efectividad. Las controversias que han limitado suindicación extendida han sido ampliamente abordadas enliteratura médica, relacionas principalmente por la ausenciaen la década de los 90 de este tipo de estudio (1 ).
Los pacientes mencionados suman la totalidad de la pobla-ción objetivo con enfermedad pulmonar crónica o DBPbroncopulmonar (DBP) , dentro del sistema público, conmayor riesgo de enfermar y morir por IRAB - VRS, sin que
hasta la fecha haya una solución programada, sistemática yregular determinando una marcada inequidad con aquellosbeneficiarios de salud del sistema privado que puedan costearesta intervención preventiva disponible sin restricciones ennuestro país.
En la Guía GES para DBP (www.minsal.cl) se hacen reco-mendaciones genéricas de prevención de la morbimortalidaden los 2 primeros años de vida. Sin incluir recomendacionesespecíficas de profilaxis para el VRS. Luego de esta publicación,la información científica disponibleha motivado su inclusión en diferentes guías clínicas interna-cionales(2,3). La Tabla 1, resume las recomendaciones de la Academia Americana de Pediatria (AAP)(1).
JUSTIFICACIÓN DEL PROGRAMA
El avance de la medicina en nuestro país, como el desarrollode las Unidades de Neonatología y el aporte de programasnacionales (surfactante, IRA, y oxigenoterapia ambulatoria),han permitido mejorar la sobrevida en forma creciente delos prematuros < de 32 semanas de edad gestacional. Noobstante, la alta tasa de reingreso durante los 2 primerosaños de vida, se traduce en un mayor riesgo de hospitalización, ventilación mecánica, letalidad y complicaciones respiratoriasen la infancia temprana y tardía.
Por otra parte, la profilaxis con anticuerpos monoclonalesanti VRS ha demostrado disminuir las tasas de hospitalizaciónen un 50% en los niños con factores de riesgo como DBP,prematuros menores de 35 semanas y lactantes con cardiopatía
congénita. En los países desarrollados y en prematurosmenores de 32 semanas de EG se logro disminuir la tasa dehospitalización por IRAB-VRS en 50% (10 a 5%)(4), llegandoincluso al 70% con una admisión del 4% en el reporte dela red de seguimiento español(7). Esta disminución promedio fue mayor en los prematuros sin DBP. En los países latinoa-mericanos la tasa de hospitalización durante el primer añode vida es significativamente mayor(20 a 30%), en Argentinalos análisis de costo efectividad considerando una reducciónhipotética de la tasa hospitalización (78% para los niños sinDBP y 39% para los niños con DBP) incorporando diferentesgrupos de riesgo señalan un NNT para impedir una hospita-lización significativamente menor (4 a 7) al haber niños
menores de 10 años y pobre escolaridad materna comparadacon la identificada en países desarrollados (NNT=16)(4).
En Chile en un seguimiento de 10 años (1994-2004) enla Región Metropolitana (SSMC) se identifico como factor deriesgo la dependencia de oxigeno. Aún cuando las tasas dehospitalización por causas respiratorias disminuyeron casi enun 50% (67% - 26%), se logro identificar al VRS en 22% delas hospitalizaciones por IRAB. Esta tasa de hospitalizaciónaumenta significativamente en los niños con PN menor de1000 gr. (Datos SSMC).
Existen 2 publicaciones internacionales recientes quedemuestran costo-efectividad en la profilaxis en contra de

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 43/54
183Prado F.
Tabla 2.- Criterios de ingreso para profilaxis VRS.
Lactante menor de 2 año con:
DBP
Oxigenodependiente (ingresado o propuesto alPrograma de Oxigeno Ambulatorio)
PRESTACIONES ENTREGADAS POR EL PROGRAMA
PROFILAXISSe utilizará profilaxis pasiva con anticuerpos monoclonaleshumanizado contra la glicoproteina F del VRS, productocomercial Palivizumab.
Características del Producto: SYNAGIS (Palivizumab)
• Palivizumab es el primer anticuerpo monoclonal huma-nizado IgG1 (inmunoglobulina) diseñado para prevenirla infección por VRS.
• Este anticuerpo monoclonal humanizado se obtiene a través de ingeniería genética (95% de secuencias ami-
noacídicas humanas y en un 5% de secuencias amino-acídicas murinas).
• Palivizumab es un anticuerpo que se une a la proteínaF del VRS.
• Palivizumab bloquea la fusión del VRS con los receptoresde las células.
• Palivizumab reduce la actividad viral y la transmisión del virus entre células.
• Palivizumab está indicado para la prevención de laenfermedad respiratoria grave baja causada por el VRSen pacientes pediátricos de alto riesgo de enfermedadpor VRS.
IRAB - VRS en niños con alto riesgo en las poblacionesanteriormente señaladas desde la perspectiva de los sistemasde salud con efectos clínicos y de costo positivos que sepodrían prolongar más allá de la temporada de VRS incluidaen la profilaxis(5,6).
La profilaxis pasiva con anticuerpos monoclonales anti
glicoproteina F del VRS, disminuye significativamente loscostos directos e indirectos al disminuir las hospitalizacionespor IRAB - VRS en los pacientes altamente susceptibles. Losestudios de costo efectividad, medida en función de los añosde vida ajustados por calidad (AVAC) ganados o QALYS(quality-adjusted life years), en distintos escenarios handemostrado una efectividad creciente para los sistemas desalud (redes sanitarias) desde una perspectiva socialmenteaceptable. A través del programa propuesto se pretendeaumentar la capacidad resolutiva de la red asistencial entregandomedidas de prevención especificas para la población deprematuros más susceptible de enfermar y morir por IRAB- VRS.
Pacientes con riesgo de enfermedad grave o potencial-mente mortal por VRS:
• Niños prematuros (<35 semanas de gestación), Mayor riesgo a menor edad gestacional.
• Niños con enfermedades pulmonares crónicas: DBP,Fibrosis quística.
• Niños con cardiopatías congénitas.
• Niños inmunocomprometidos.
Factores de riesgo que facilitan la infección:• Hermanos en edad escolar.
• Pobre escolaridad materna.
• Guarderías.
• Contaminación ambiental, tabaquismo.
• Ausencia lactancia materna o menor a 3 meses.
• Menor 10 semanas al momento temporada VRS.
EL OBJETIVO
Consiste en disminuir los costos directos por hospitalizaciónrelacionados con IRAB - VRS para el sistema de salud público(MINSAL) y los costos indirectos derivados por la asociaciónde sibilancias a repetición y asma en la primera infancia conun apropiado efecto costo-efectividad.
El Programa consiste en la administración mensual dePalivizumab intramuscular en forma ambulatoria durante la temporada VRS como estrategia complementaria a la Cam-paña de Invierno en 100 prematuros con DBP menores de2 años incluidos en el Programa de Oxigenoterapia Ambula- torio, cifra que corresponde a la totalidad de niños prematuroscon mayor riesgo de enfermar y morir por IRAB - VRS, según
catastro efectuado por el Programa IRA del Minsal (2007,datos del Registro del Programa Chileno de Oxigenoterapia Ambulatoria) . Durante la campaña de invierno 2008 seentregara profilaxis a 40 niños con DBP, < de 1 año ydependientes de oxigenoterapia.
COBERTURAS
En virtud de los análisis de costo efectividad en poblacionescon riesgos sociales similares a los nuestros (Argentina -España) y considerando que independiente del nivel dedesarrollo de los países el grupo de mayor riesgo de enfermary morir son los lactantes con DBP, menores de 2 años ydependientes de oxigeno se platea como grupo target paraprofilaxis VRS en este piloto a los niños con las característicasseñalada en la tabla 2.

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 44/54
REFERENCIAS:
1. Stevens T, Hall C. Controversie s in Palivizumab Use. Pediatr Infect Dis J2004;23:1051-1052.
2. Comité de Estudios Fetoneonatales (CEFEN ) Actualización de las recomendacionessobre el uso de palivizumab. Arch Argent Pediatr 2007; 105(1):67-70
3. Figueras J, Querob J. Comité de Estándares de la Sociedad Española de Neonatología.Recomendaciones para la prevención de la infección por virus respiratorio sincitial. An Pediatr (Barc) 2005;63(4):357-62
4. The IMpact-RSV Study Group. Pediatrics. 1998;102:531-537.5. Lázaro P, Figueras J, Doménech E, Echániz I, Closa R, Wood M.A, Fitch K La
eficiencia (coste-efectividad) de palivizumab como profilaxis para la infección por virus respiratorio sincitial en prematuros de 32-35 semanas en España. An Pediatr(Barc). 2006;65(4):316-24.
6. Nuijten MJ, Wittenberg W, Lebmeier M. Cost effectiveness of palivizumab forrespiratory syncytial virus prophylaxis in high-risk children: a UK analysis.
Pharmacoeconomics.2007;25:55-71.7. Pedraz C, Carbonell X, Figueras-Aloy J, Quero J, the IRIS Study Group. Effectiveness
of palivizumab prophylaxis in decreasing syncytial virus hospitalizations in prematureinfants. Pediatr Infect Dis J.2003;22:823-827.
184
Anexo A.- Distribución niños < 2 años con DisplasiaBroncopulmonar con oxigeno domiciliario
Servicio SaludNiños con Niños conDisplasia Displasia
menor 1 año menor 2 años
Metro Central 10 13
Metro Norte 8 9
Metro Occidente 7 7
Metro Sur 12 15
Metro Sur Oriente 19 22
Metro Oriente 9 11
Hospital Josefina Martinez
2 5
Total 67 83
Fuente: Programa Nacional de Oxigeno Ambulatorio, sobre un total de226 pacientes a julio 2007.
Programa de profilaxis VRS en niños con displasia broncopulmonar en Atención Primaria de Salud
• L a seguridad y la eficacia fueron establecidas en lactantescon DBP, lactantes con historia de prematurez (35semanas o menos de edad gestacional), y niños concardiopatía congénita hemodinámicamente significativa.
PRESENTACIÓN
• Viales de 50 ó 100 mg. de polvo liofilizado.
• Cada vial tiene suficiente producto para cubrir las nece-sidades de:
- Un niño de 6.6 Kg. de peso durante un mes(100 mg).
- Un niño de 3.3 Kg. de peso durante un mes(50 mg).
DOSIFICACIÓN
• 15 mg/Kg peso (administración en sus domicilios).
• Vida media de 30 días, por lo que su dosificación es una vez al mes. La primera dosis se administra antes delinicio de la temporada del VRS en la comunidad, y lasdosis sucesivas a intervalos mensuales hasta fin de temporada. (máximo 5 dosis). La primera dosis ideal-mente debe ser administrada 3 días antes del alta deneonatología.
SERVICIO COMPLEMENTARIO (FULL SERVICE)
Servicios Adicionales asociados a la venta del producto:
• Despacho oportuno del producto al lugar donde serealizará la inmunización.
• Manejo de base de datos de pacientes (sofware deregistro y análisis estadístico).
• Manejo logístico:
• Chequeo del listado de pacientes que deben recibir Synagis:
- Chequeo de los datos del paciente.
- N° de dosis que corresponde recibir.
- Fecha de inmunización.
- Teléfono de contacto.
• Chequeo del n° de viales disponibles para asegurarque todos los pacientes puedan recibir su dosis.
• Material de apoyo en la jornada de inmunización:
- Ficha paciente.
- Tarjeta de control de inmunización.
- Ficha para registro de nuevos pacientes.
- Ficha para registro de pacientes en dosis subsi-guientes.
- Ficha para registro de asistencia (cumplimiento)
• Asesoría y atención telefónica personalizada a los padreso representantes de los pacientes.
• Entrega de material de apoyo para padres.
• Contacto telefónico con los padres de los pacientes 2días antes, para recordar la fecha de la próxima inmuni-zación.
• Inmunización en el domicilio.
• Enfermera coordinadora de seguimiento.

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 45/54

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 46/54
186 Estudio de costo-efectividad de la profilaxis VRS en Chile
presenta como una infección respiratoria alta leve, pero hastael 2% de los lactantes requiere ser hospitalizado en el áreanorte de Santiago(2). La epidemia de VRS ocurre cada año yes responsable del 50 a 80% de las hospitalizaciones duranteel invierno. El promedio de duración de las epidemias duranteel invierno va entre 3.5 y 5.5 meses y se extienden entre
mayo y septiembre en Chile(2,3,4,5)
. Hemos descrito 2 tiposde epidemias en nuestro país, que aparecen año por medio:una de inicio precoz y se extiende por 3 meses y la otracomienza más tarde y dura 5.5 meses(2)
En pacientes con enfermedades de base, tales como DBPo enfermedad pulmonar crónica del prematuro, cardiopatíascongénitas y prematurez, la bronquiolitis o neumonía por VRS puede transformarse rápidamente en una enfermedadsevera y requerir hospitalizaciones prolongadas y muer- tes(16,17,18) . Se ha demostrado que los prematuros hospitali-zados por una infección por VRS requieren 50% más decuidados en unidades especializadas, tres veces más de usodel recurso kinesiólogo, y se hospitalizan 8 veces más fre-
cuentemente en el período de seguimiento post alta porenfermedades respiratorias y tienen 5 veces más riesgo demorir (19,20).
En Chile, la hospitalizaciones por infección por VRS en 75lactantes con DBP nacidos entre 1995 y 2001 en el áreanorte de Santiago y seguidos por 2 años fue de 21%(21). Lospacientes portadores de DBP están también en riesgo deinfecciones por adenovirus nosocomial que son más severasy fatales. En nuestra cohorte de pacientes la tasa de morta-lidad durante el seguimiento fue de 7%, no asociado al VRSdirectamente, pero si al motivo de hospitalización que facilitóla adquisición de la infección intrahospitalaria por adenovirus.
En la cohorte de Sampalis en Canadá, la mortalidad global fue de 8.1% versus 1.6% en los lactantes hospitalizados poruna IRAB no VRS, excluyendo el evento índice(20).
Los prematuros que presentan una bronquiolitis por VRSprecozmente en la vida tienen mayor riesgo de sibilanciasrecurrentes.(23) Recientemente un estudio sugiere que laprevención de la infección por VRS con palivizumab puedereducir las sibilancias recurrentes en lactantes prematuros24.En nuestro seguimiento de prematuros con displasia bronco-pulmonar en el área norte de Santiago durante 2 años seencontró la presencia de al menos un episodio de sibilanciasen 53% y de atelectasias crónicas en 22%. Las atelectasiasson también una complicación frecuente de la IRAB por VRSque demanda kinesioterapia respiratoria. El manejo de laDBP en Chile está estandarizado de acuerdo a normasnacionales (GES) Los pacientes reciben la vacuna antigripaly antineumocócica.
La prevención del VRS se basa en la educación de lospadres sobre la importancia de reducir la exposición del niñoa la infección y la profilaxis pasiva. Desde 1996 existe disponiblela immunoglobulina endovenosa (RSV-IGIV)(24,25) y los anti-cuerpos monoclonales humanizados preparados sobre laglicoproteína F del VRS (palivizumab, Synagis®).
La US Food and Drug Administration (FDA) aprobó el usode palivizumab en 1998 para la prevención de la IRAB por
VRS en niños de alto riesgo, en administración mensualintramuscular. Los resultados de dos ensayos terapéuticosrandomizados controlados doble ciego con palivizumab, queincluyeron 2789 lactantes y niños prematuros, con DBP ocardiopatías congénitas demostraron una reducción de la tasade hospitalización por VRS de 39% a 78% en diferentes
grupos(1,26)
L os resultados de estudios observacionales postlicencia, sugieren que la inmunoprofilaxis mensual con palivi-zumab podría reducir las tasas de hospitalización por IRABpor VRS incluso mayores (70%) que las reportadas en losensayos clínicos controlados(27) El estudio IMpact no fuediseñado para investigar mortalidad(1).
La Academia Americana de Pediatría ha publicado guíasclínicas para la selección de pacientes de alto riesgo que sebeneficiarían con la inmunoprofilaxis mensual con palivizu-mab (28,29). Es claro que la profilaxis con palivizumab esbeneficiosa26,1. El impacto económico ha sido evaluado conestudios de costo-efectividad, con diferentes efectos medidos:reducción del número y días de hospitalizaciones y años de
vida ganados. Existe una gran variabi lidad en estos estudiosque en Chile no se han efectuado(30-39).
Basado en el supuesto de que utilizando palivizumab anuestra cohorte de pacientes con DBP seguidos, podríamoshaber reducido la tasa de hospitalización desde 20 a 10% en vez de 10 a 5% como lo demostró el estudio IMpact(1),podríamos hipotetizar que en nuestro país, la profilaxis de VRS a niños de alto riesgo podría se eficiente. En la poblaciónde pacientes analizados en el estudio IMpact es necesario tratar 16 pacientes con palivizumab para evitar una hospitali-zación) (Número necesario a tratar o NNT)(1). MINSAL haestimado los costos de cada hospitalización para cada uno
de estos niños $1.000.000, lo que no corresponde a lo real.Es importante contar con valores reales para poder realizarestudios de palivizumab.
Un aspecto crucial en la prevención de lactantes de altoriesgo es la educación de los padres y cuidadores sobre laimportancia de disminuir la exposición de niños al VRS. Losniños de alto riesgo deben ser excluidos de situaciones dondela exposición a personas infectadas no puedan ser controladas, tales como salas cunas. El énfasis está en el lavado de manosen todo momento, incluyendo la casa y en evitar la exposiciónal tabaquismo pasivo(14).
Para el año 2008, el MINSAL decidió iniciar un programa
piloto de profilaxis de VRS con palivizumab en 40 lactantesmenores de 1 año portadores de DBP y oxígeno dependenciaen el área sur oriente en Santiago. La decisión tomada sebasó en la información disponible de que el área sur-orientees la más vulnerable y corresponde al 30% aproximado dela población que atiende FONASA. La inmunización se haráen los domicilios y estará a cargo de una enfermera. Estasituación nos obliga a comparar la evolución de las cohortesde beneficiados y no. En otras circunstancias esto no seríaposible desde el punto de vista ético.
Nuestra hipótesis a demostrar es que la intervención conSynagis® en lactantes con DBP en Chile es costo-efectiva. Veremos menor morbilidad aguda y a largo plazo en el grupo

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 47/54
187Palomino M. et al
protegido y los costos asociados a la profilaxis de la infecciónpor VRS serán al menos igual o menor que los costos de lacohorte no intervenida. Si esta hipótesis es verdad, MINSALpodría extender la profilaxis a otros niños de alto riesgo segúnlas recomendaciones de la AAP(28,29).
REFERENCIAS
1. The IMPACT RSV study group. Palivizumab, a humanized RSV monoclonal antibody,reduces hospitalization from RSV infection in high-risk infants. Paediatrics 1998;102: 531-7.
2. Avendaño LF, Larrañaga C, Palomino MA, et al. Community- and hospital -acquiredrespiratory syncytial virus infection in Chile. Pediatr Infect Dis J 1991; 10: 564-8.
3. Avendaño L F, Palomino M A, Larrañaga C. Surveillance for Respiratory Syncytial Virus in infants hospitalized for acute lower respiratory infection in Chile (1989 to2000). J Clin Microbiol 2003; 41: 4879-82.
4. Palomino MA, Avendaño L. Infecciones respiratorias por VRS y adenovirus enChile: qué hemos aprendido en 14 años de vigilancia epidemiológica. Rev Pediatr(Santiago) 2003; 46: 38-47.
5. Palomino MA, Larrañaga C, Montaldo G, Suárez M, Díaz A, Avendaño LF. Infecciónextra e intrahospitalaria por virus sincicial respiratorio en lactantes. Rev Chil Pediatr1994; 65: 11-16.
6. Girardi B, Astudillo O, Zúñiga F. El programa IRA en Chile: hitos e historia. Rev
Chil Pediatr 2001; 72: 292-300.7. Kaempffer AM, Medina E. Mortalidad infantil reciente en Chile: éxitos y desafíos.Rev Chil Pediatr 2006; 77: 492-500.
8. Young P. White House to expand response to infectious diseases. ASM News1996; 62: 450-1.
9. Lagos R, Avendaño LF, Levine M. Vigilancia sistemática de virus influenza, respiratoriosincicial, parainfluenza y adenovirus en niños ambulatorios con infecciones agudasrespiratorias. Rev Méd Chile 1999; 127:1063-72.
10. Larrañaga C, Kajon A, Villagra E, Avendaño LF. Adenovirus surveillance on childrenhospitalized for acute lower respiratory infections in Chile (1988-1996). J Med Virol 2000; 60: 342-6.
11. Palomino MA, Larrañaga C, Avendaño LF. Hospital-acquired adenovirus 7h infantilerespiratory infection in Chile. Pediatr Infect Dis J 2000; 19: 527-31.
12. Palomino MA, Larrañaga C, Villagra E , Camacho J, Avendaño LF. Adenovirus andrespiratory syncytial virus-Adenovirus mixed acute lower respiratory infections inChilean infants. Pediatr Infect Dis J 2004; 23: 337-41.
13. Larrañaga C, Martínez J, Palomino MA, Peña M, Carrión F, Avendaño LF. Molecularcharacterization of hospital-acquired adenovirus infantile respiratory infection inChile using species-specific PCR assays. J Clin Virol 2007; 39: 175-81.
14. Hall CB. Respiratory syncytial virus and parainfluenza virus. N Engl J Med 2001;344: 1917-28.
15. McIntosh K. Respiratory syncytial virus infections in infants and children: diagnosisand treatment. Pediatr Rev 1987; 9: 191-6.
16. Groothuis JR, Gutierrez KM, Lauer BA. Respiratory syncytial virus infection inchildren with bronchopulmonary dysplasia. Pediatrics 1988; 82:199-203.
17. Cunningham CK, McMillan JA, Gross SJ. Rehospitalization for respiratory illness ininfants less than 32 weeks' gestation. Pediatrics 1991; 88: 527-532.
18. Meissner HC. Selected populations at increased risk from respiratory syncytial virusinfection. Pediatr Infect Dis J (2003) 22: pp S40-S45.
19. Welliver RC. Review of epidemiology and clinical risk factors for severe respiratorysyncytia l virus (RSV) infection. J Pediatr 2003; 143: S112-S117.
20. Sampalis JS. Morbidity and mortality after RSV-associated hospitalizations amongpremature Canadian infants. J Pediatr 2003; 143: S150-S156.
21. Palomino MA, Morgues M, Martinez F. Management of infants wi th chronic lungdisease of prematurity in Chile. Early Human Development 2005; 81: 143-149.
22. Pérez-Yarza EG, Moreno A, Lázaro P, Mejías A, Ramilo O. The association betweenrespiratory syncytial virus infection and the development of childhood asthma: asystematic review of the literature. Pediatr Infect Dis J 2007; 26: 733-9.
23. Pedraz C, Carbonell X, Figueras-Aloy J, Quero J, the IRIS Study Group. Effectivenessof palivizumab prophylaxis in decreasing syncytial virus hospitalizations in prematureinfants. Pediatr Infect Dis J 2003; 22: 823-827.
24. Meissner HC, Groothuis JR. Immunoprophylaxis and the control of respiratorysyncytial virus disease. Pediatrics 1997; 100: 260 -263.
25. Meissner HC, Long SS. Revised indications for the use of palivizumab and respiratorysyncytial virus immune globulin intravenous for the prevention of respiratory syncytial virus infection. Pediatrics 2003; 112: pp 1447-1452.
26. Feltes TF, Cabalka AK, Meissner HC, and Cardiac Synagis study group Palivizumabprophylaxis reduces hospitalization due to respiratory syncytial virus in youngchildren with hemodynamically significant congenital heart disease. J Pediatr (2003)143: pp 532-540.
27. Romero J.R. Palivizumab prophylaxis of respiratory syncytial virus disease from1998 to 2002: results from four years of palivizumab usage. Pediatr Infect Dis J2003; 22: S46-S54.
28. American Academy of Pediatrics, Committee on Infectious Diseases and Committeeon Fetus and Newborn. Prevention of respiratory syncytial virus infections: indications for the use of palivizumab and update on the use of RSV-IGIV. Pediatrics 1998;102: 1211-1216.
29. American Academy of Pediatrics, Committee on Infectious Diseases and Committeeon Fetus and Newborn. Revised indications for the use of palivizumab and respiratorysyncytial virus immune globulin intravenous for the prevention of respiratory syncytial virus infections. Pediatrics 2003; 112: 1442-1446.
30. Lázaro P, Figueras J, Doménech E, Echániz I, Closa R, Wood MA, Fitch K. Laeficiencia (coste-efectividad) de palivizumab como profilaxis para la infección por virus respiratorio sincitial en prematuros de 32-35 semanas en España. An Pediatr(Barc) 2006; 65: 316-24.
31. Pedraz C, Carbonell X, Figueras-Aloy J, Quero J and the IRIS Study Group.
Effectiveness of palivizumab prophylaxis in decreasing syncytial virus hospitalizationsin premature infants. Pediatr Infect Dis J 2003; 22: 823-827.32. Nuijten MJ, Wittenberg W, Lebmeier M. Cost effectiveness of palivizumab for
respiratory syncytial virus prophylaxis in high-risk children: a UK analysis.Pharmacoeconomics 2007; 25: 55-71.
33. Kamal-Bahl S, Doshi J, Campbell J. Economic analysis of respiratory syncytial virusimmunoprophylaxis in high-risk infants: a systematic review. Arch Pediatr AdolescMed 2002; 156: 1034-1041.
34. Lofland UH, O'Connoe JP, Chatterton ML, et al. Palivizumab for respiratory syncytial virus prophylaxis in high-risk infants: a cost-effectiveness analysis . Clin Ther 2000;22: 1357-1369.
35. Shireman TI, Braman KS. Impact and cost-effectiveness of respiratory syncytial virus prophylaxis for Kansas Medicaid's high-risk children. Arch Pediatr Adolesc Med2002; 156: 1251-1255.
36. Numa A. Outcome of respiratory syncytial virus infection and cost-benefit analysisof prophylaxis. J Paediatr Child Health 2000; 36: 422-427.
37. Joffe S, Ray GT, Escobar GJ, et al. Cost-effectiveness of respiratory syncytial virusprophylaxis among preterm infants. Pediatrics 1999; 104: 419-427.
38. Roeckl-Wiedmann T, Liese JG, Grill E, et al. Economic evaluation of possible
prevention of RSV-related hospitalizations in premature infants in Germany. Eur JPediatr 2003; 162: 237-244.
39. Prais D, Schonfeld T, Amir J. Admissions to the intensive care unit for respiratorysyncytial virus bronchiolitis: a national survey before palivizumab use. Pediatrics2003; 112: 548-552.
40. www.MINSAL.cl esta referencia esta mal citada. Falta colocar además la fecha derevisión
41. www.prematuros.cl esta referencia esta mal citada. Falta colocar además la fechade revisión
42. Comité de Estudios Fetoneonatales (CEFEN) Actualización de las recomendacionessobre el uso de palivizumab. Arch Argent Pediatr 2007; 105: 67-70.
43. Figueras J, Querob J. y Comité de Estándares de la Sociedad Española deNeonatología. Recomendaciones para la prevención de la infección por virusrespiratorio sincicial. An Pediatr (Barc) 2005; 63: 357-62.

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 48/54
disponible en http://www.neumologia-pediatr ica.cl188
NEUMOLOGIA PEDIATRICA ISSN 0718-3321
¿Tendremos una vacuna contra el VRS?
Dr. Luis Fidel AvendañoPediatra InfectólogoHospital San Borja Arriarán
No obstante que existe la convicción que la vacuna sería elarma más poderosa de prevención, o que existe un mejorconocimiento de la biología del virus respiratorio sincicial(VRS), o que hay sistemas de diagnóstico de VRS muy difun-didos, o que hay muchos grupos de científicos trabajando enel tema, no se vislumbra una vacuna en un futuro cercano.
PROBLEMAS DERIVADOS DE LA PATOGENIA DEL
VRS
a) Contagio a temprana edad por alta contagiosidad. Serequiere vacunación precoz.
b) Mala respuesta inmune natural, pues existen re-infeccionesen niños y adultos La vacuna debería ser mejor inductora deinmunidad que la infección natural ¿qué ejemplo hay? Estosdos puntos representan un problema estratégico para desa-rrollar y probar un candidato de vacuna en la poblaciónblanco, que son los lactantes antes que se infecten y ojalaseronegativos.
c) Aunque no hay tratamiento específico, se ha bajado lamortalidad mejorando el manejo clínico y epidemiológico,pero no se ha controlado la aparición de brotes epidémicos.
d) L a quimioprofilaxis (anticuerpos monoclonales humani-zados) tiene aplicación muy restringida. Estos avances en terapia y quimioprofilaxis son valiosos, pero no influyen enla forma de presentación de los brotes, que igual sigueafectando anualmente a no menos del 60% de los niñosnacidos en el año.
e) La infección en adultos e inmunocomprometidos pareceser relevante. Se han agregado dos nuevas poblaciones blancode vacunación, resaltando la importancia del VRS comopatógeno en adultos.
PROBLEMAS PARA DESARROLLO DE VACUNA
a) Infección temprana: Inmadurez inmunológica (respuestaLTh1/2, LTc): Una vacuna debería inducir buen nivel deanticuerpos neutralizantes e inmunidad celular de LTh1 ycitotóxica, para remedar la respuesta que se obtiene en formanatural, posiblemente después de varios contactos con el virus.
b) Beneficio/interferencia de anticuerpos maternos: Nohay duda que los anticuerpos transmitidos pasivamente porla madre protegen al hijo, hecho base de la inmunoprofilaxiscon monoclonales humanizados. Sin embargo, se ha demos- trado que la presencia de anticuerpos maternos interfierecon el desarrollo de una respuesta inmune adecuada.
c) Vacuna inactivada con formalina tuvo efecto negativo enla década del 60. Hoy día hay explicaciones para ese fenómeno
(respuesta Th2, ausencia de anticuerpos neutralizantes) y uncandidato de vacuna debe demostrar primero que es inocuo,
antes de seguir probando la inmunogenicidad.
d) Patogenia no aclarada y variabilidad antigénica: proteínasF y G. Se ha definido que la inmunidad depende de las dos
glicoproteínas de superficie F y G. La proteína F es muyconservada y es la meta para preparar vacunas; la gpG es
variable y permit iría entender variaciones epidemiológicas.
Una vacuna debería inducir anticuerpos neutralizantes contraF y una respuesta tipo Th1, talvez dependiente de G.
ESTRATEGIAS DESARROLLO VACUNA VRS
Chile tiene tradición de buen país para estudiar y usar vacunas.
a) Vacunas no infectivas (subunidades): FI-RSV, PFP1-2-3.La forma más fácil de preparar una vacuna en inactivando el virus completo por medios físicos o químicos. También sepueden purificar los componentes inmunogénicos superficiales(subunidades) o hacer en forma biosintética.
b) Vacunas vivas atenuadas: La forma tradicional de atenua-ción ha sido por pasaje del virus en huéspedes no habituales,probando periódicamente la toxicidad e inmunogenicidad delas cepas resultantes. Se pueden usar agentes mutagénicoscomo alternativa del proceso de selección natural.
c) Biología molecular: puede aplicarse para desarrollarambas estrategias. El gran avance de la biología molecularpermite actualmente preparar antígenos en forma biosintética;insertar genes codificantes de antígenos en vectores micro-bianos; atenuar cepas por modificación de su genoma;preparar cepas quimeras para diversos antígenos; prepararcepas recombinantes por supresión y agregado de genes ypropagarlas en diversos vectores (MEDI-534).
d) Adyuvantes: ISCOM. La forma de presentación delantígeno parece vital en el tipo de inmunidad a inducir, y losadyuvantes podrían modular y mejorar la respuesta inmune.
Cualquier candidato deberá avanzar progresivamentesuperando primero pruebas de tolerancia e inmunogenicidada diferentes dosis, y protección in vivo en animales; luego,en individuos humanos en grupos pequeños (tolerancia einmunigenicidad: fases I y II), y después en grupos más grandes(inmunodeficiencias + eficacia: fase III); finalmente, una vezaprobada formalmente la fase III, se estudia la eficacia encomunidades (fase IV). Una buena estrategia para mejorar lainmunidad pasiva podría ser la vacunación de embarazadas.

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 49/54
LECTURAS RECOMENDADAS
1. Openshaw PJ, Tregoning JS. Immune responses and disease enhancement duringRespiratory Syncytial Virus Infection. Clin Microbiol Rev 2005; 18: 541-555.
2. Avendaño L F, Palomino M A, Larrañaga C. Surveillance for Respiratory Syncytial Virus in infants hospitalized for acute lower respiratory infection in Chile (1989 to2000).J Clin Microbiol 2003; 41: 4879-82
3. Piedra PA, Clinical experience with respiratory syncytial virus vaccines. Pediat InfectDis J 2003; 22: S94-9.
4. Muñoz FM, Piedra PA, Glezen WP. Safety and immunogenicity of respiratorysyncytial virus purified protein-2 vaccine in pregnant woman. Vaccine 2003; 21:3465-7.
5. Piedra P. Future directions in vaccine prevention of respiratory syncytial virus. PedInfect Dis J 2002; 21:482-7.
6. Dudas RA, Karron RA. Respiratory Syncytial Virus Vaccines. Clin Microbiol Rev1998; 11: 430-449.
7. Morein B, Sundquist B, Höglund SW, Dalsgaard K, Osterhaus A. ISCOMs, a novelstructure for antigenic presentation of membrane proteins from enveloped viruses.Nature 1984; 308: 457-60.
8. Hagglund S, Hu KF, Larsen LE, et al. Bovine respiratory syncytial virus ISCOMs--protection in the presence of maternal antibodies. Vaccine 2004; 23: 646-55.
9. Belshe RB, Newman FK, Anderson EL, et al. Evaluation of combined live, attenuatedrespiratory syncytial virus and parainfluenza 3 virus vaccines in infants and youngchildren. J Infect Dis 2004; 190: 2096-2103.
10. Safety and tolerability study to evaluate MEDI-534 in children 6 to <24 monthsof age. http://clinicaltrialsfeeds.org/clinical-trials/show/NCT00493285
189¿Tendremos una vacuna contra el VRS?
Actualmente hay muchos candidatos en etapas iniciales ypocos en fase III. La vacuna contra el sarampión -otro para-mixovirus, más clásico en su patogenia y forma de presenta-ción- se empezó a aplicar en Chile en 1964 y sólo 40 añosdespués se logra controlarlo en nuestro país, no en las Américas, ni en el mundo. ¿Cuánto se demoraría en hacerlo
una futura vacuna anti VRS?

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 50/54
CALENDARIO CIENTIFICO SOCHINEP 2008
Curso de especialistas: Novedades del VRS viernes 9 y sábado 10 de Mayo
Con la participación del Dr. Octavio Ramilo (Dallas)
Congreso SOCHINEP 2008 jueves 16, viernes 17 y sábado 18 de octubre
Con la participación de Dr. Félix Ratjen (Toronto): Fibrosis quísticaDr. Manuel Soto Quirós (Costa Rica): Genética y epidemiología del asmaDr .Christian Poets (Alemania): Estudios de sueño
Reuniones Mensuales SOCHINEPReuniones mensuales (primer jueves de cada mes)
Hospital Clínico Universidad Católica(*) 13 de MarzoHospital Padre Hurtado 3 de Abril
Hospital de Antofagasta (por confirmar) 8 de MayoHospital Josefina Martínez 5 de Junio
Hospital Carabineros 3 de Julio
Hospital Gustavo Fricke 7 de AgostoHospital Sótero del Río 4 de SeptiembreClínica Las Condes 2 de Octubre
Hospital San Borja Arriarán(*) 13 de NoviembreHospital Ezequiel Gonzalez Cortés 4 de Diciembre
(*) segundo jueves del mes
OTRAS ACTIVIDADES CIENTÍFICAS 2008
INTERNATIONAL CONGRESS ON PEDIATRIC PULMONOLOGY (CIPP VIII)8° Congreso Internacional de Neumología Pediátrica, 29-31 de Marzo
Nice, Francia27º JORNADAS DE OTOÑO
Sociedad Chilena de Enfermedades RespiratoriasImagenología en Enfermedades Respiratorias: Niños y Adultos
04 y 05 de Abril
AMERICAN THORACIC SOCIETY (ATS)Conferencia Internacional, 16-21 de Mayo
Toronto, Canadá
ICPP 4, THE COURSE
IV Curso Internacional de Neumología Pediátrica, 12-14 de JunioPortofino, Italia
17º JORNADAS DE INVIERNOSociedad Chilena de Enfermedades Respiratorias
Infecciones Respiratorias, Tuberculosis y Sida, en niños y adultos4 y 5 de Julio
EUROPEAN RESPIRATORY SOCIETY (ERS)Conferencia Internacional, 4-8 de Octubre
Berlin, Alemania
41º CONGRESO CHILENO DE ENFERMEDADES RESPIRATORIASSociedad Chilena de Enfermedades Respiratorias
05 al 08 de Noviembre

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 51/54
La Revista Neumología Pediátrica es el órgano oficial de difusión de la Sociedad Chilena de Neumología Pediátricay publica temas de revisión en torno a la salud respiratoria infantil y del adolescente. Los trabajos enviados a nuestrarevista que cumplen con los requisitos solicitados, son sometidos a arbitraje por médicos investigadores y expertosde nuestro medio. Nuestro comité editorial consulta y selecciona temas, opiniones, polémicas o controversiasde actualidad general del medio pediátrico respiratorio. Los trabajos pueden enviarse por formato electrónico ao en su defecto a LE. Vega-Briceño, Editor Responsable. Revista Neumología Pediátrica. Lira 85 5to. Piso. LaboratorioRespiratorio. Santiago Centro. Casilla 114-D, Chile.
INSTRUCCIONES PARA AUTORES
El trabajo debe ser escrito en papel tamaño carta (21,5 x 27,5 cm), dejando un margen de al menos 2,5 cm enlos 4 bordes. Todas las páginas deben ser numeradas en el ángulo superior derecho, empezando por la página
del título. Debe entregarse dos ejemplares idénticos de todo el texto, con las Referencias, Tablas y Figurasacompañados por una copia idéntica para PC, en CD o diskette de 3,5 con espaciado a 1,5 líneas; tamaño de letra12 pt y justificada a la izquierda. Las Figuras que muestren imágenes (radiografías, histología, etc.) deben entregarseen copias fotográficas. Los trabajos enviados no deben sobrepasar de 3000 palabras, pudiendo agregárseles hasta4 tablas y 2 figuras y no más de 40 referencias en lo posible. Las Cartas al Editor u Opiniones no deben exceder1.000 palabras, pudiendo agregárseles hasta 6 referencias y 1 Tabla o Figura.
El título del trabajo debe ser conciso pero informativo sobre el contenido central de la publicación; El o los autoresdeben ser identificados con su nombre de pila seguido del apellido paterno. Debe de colocarse el nombre de lao las Secciones, Departamentos, Servicios e Instituciones a las que pertenece actualmente el o los autoresresponsables; el nombre y dirección del autor con quien establecer correspondencia, incluir un número de fax ycorreo electrónico. Exprese su agradecimiento sólo a personas e instituciones que hicieron contribuciones substantivasa su revisión. Los autores son responsables por todas las ideas expresadas y sus conclusiones.
El límite las referencias es idealmente 40; prefiera las que correspondan a trabajos originales registradas en elPubMed. Numere las referencias en el orden en que se las menciona por primera vez en el texto. Identifíquelasmediante numerales arábigos, colocados (entre paréntesis) al final de la frase o párrafo en que se las alude. Losresúmenes de presentaciones a Congresos pueden ser citados como referencias sólo cuando fueron publicadosen revistas de circulación. Cada tabla deberá ir en hojas a parte. Numere las tablas en orden consecutivo y asígnelesun título que explique su contenido sin necesidad de buscarlo en el texto del manuscrito (título de la tabla). Sobrecada columna coloque un encabezamiento corto o abreviado. Cuando se requieran notas aclaratorias, agréguelasal pie de la tabla. Use notas aclaratorias para todas las abreviaturas no estándar. Cite cada tabla en su ordenconsecutivo de mención en el texto. Las figuras podrán ser dibujos o diseños mediante un programa computacional.Envíe 2 reproducciones de cada figura, en blanco y negro (tamaño 9x12 cm). Las letras, números, flechas o símbolosdeben verse claros y nítidos y deben tener un tamaño suficiente como para seguir siendo legibles cuando la figurase reduzca de tamaño. Sus títulos y leyendas no deben aparecer en la figura, sino que se incluirán en hoja aparte.
En el respaldo de cada figura debe anotarse con lápiz de carbón o en una etiqueta, el número de la figura, elnombre del autor principal. Cite cada figura en el texto en orden consecutivo. Si una figura reproduce materialya publicado, indique su fuente de origen. Presente los títulos y leyendas de las tablas y figuras en una páginaseparada.
Cuerpo Editorial
N E U M O L O G I A
P E D I A T R I C A

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 52/54

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 53/54
La asociación de Ipratropio y ß2 agonistadisminuye la presencia de efectos
adversos como taquicardia y temblor
Protege contra el broncoespasmoinducido por el ejercicio
Respuesta broncodilatadorasuperior a monoterapias conß2 agonistas
Previene la aparición debroncoespasmos nocturnos
Doble acción - Doble eficacia
Mayor efecto y duraciónbroncodilatadora
No genera reacciones
alérgicas en
pacientes sensibles
a la lecitina
de soya
®
v e c e s a l d í
a 3 3
Bromuro de Ipratropio + Bromohidrato de Fenoterol
Referencia:1.- Beakes 1997; Journal of Asthma 34(5): 357-368.2.- Wright y Martin 1995; Postgraduate Medicine vol 97 N˚ 6.

7/21/2019 aparato repirato
http://slidepdf.com/reader/full/aparato-repirato 54/54
Línearespiratoria
abcd